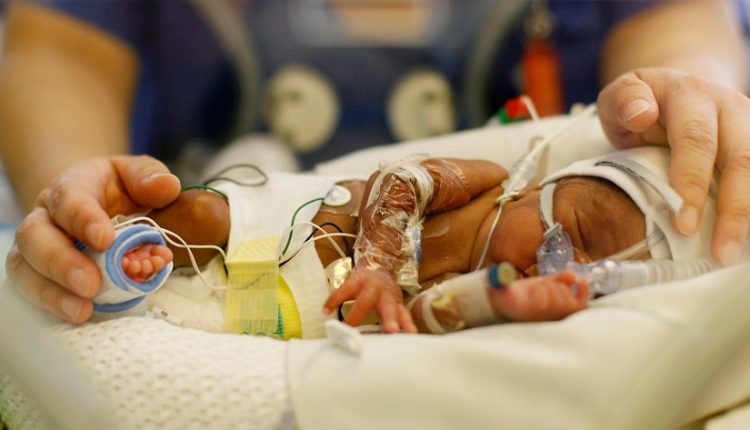
Notfallpädiatrie / Neugeborenes Atemnotsyndrom (NRDS): Ursachen, Risikofaktoren, Pathophysiologie
Das neonatale Atemnotsyndrom (NRDS) ist ein respiratorisches Syndrom, das durch das Vorhandensein einer fortschreitenden Lungenatelektase und respiratorischer Insuffizienz gekennzeichnet ist und hauptsächlich bei Frühgeborenen diagnostiziert wird, die noch nicht die vollständige Lungenreife und ausreichende Surfactant-Produktion erreicht haben
Synonyme für das Säuglings-Atemnotsyndrom sind:
- ARDS des Säuglings (ARDS steht für akut Atemstörung Syndrom);
- ARDS des Neugeborenen;
- Neugeborenes ARDS;
- pädiatrisches ARDS;
- neonatales RDS (RDS steht für „Atemnotsyndrom“);
- neugeborenes Atemnotsyndrom;
- akutes Atemnotsyndrom des Kindes;
- akutes Atemnotsyndrom des Neugeborenen.
Das Atemnotsyndrom war früher als „Hyaline Membran Disease“ bekannt, daher das Akronym „MMI“ (jetzt nicht mehr verwendet).
Das Infant Respiratory Distress Syndrome heißt auf Englisch:
- infantiles Atemnotsyndrom (IRDS);
- Atemnotsyndrom des Neugeborenen;
- neonatales Atemnotsyndrom (NRDS);
- Surfactant-Defizit-Störung (SDD).
Das Syndrom war früher als „Hyaline Membran Disease“ bekannt, daher das Akronym „HMD“.
Epidemiologie des Neugeborenen-Atemnotsyndroms
Die Prävalenz des Syndroms beträgt 1-5/10,000.
Das Syndrom betrifft etwa 1 % der Neugeborenen.
Die Inzidenz nimmt mit fortschreitendem Gestationsalter ab, von etwa 50 % bei Kindern, die in der 26. bis 28. SSW geboren wurden, auf etwa 25 % bei der 30. bis 31. SSW.
Das Syndrom tritt häufiger bei Männern, Kaukasiern, Säuglingen diabetischer Mütter und zweitgeborenen Frühgeborenen auf.
Obwohl es viele Formen von respiratorischer Insuffizienz gibt, die Neugeborene betreffen, ist NRDS die vorherrschende Ursache bei Frühgeborenen.
Fortschritte bei der Prävention von Frühgeburten und der Behandlung von neonatalem NRDS haben zu einer signifikanten Verringerung der Zahl der Todesfälle aufgrund dieser Erkrankung geführt, obwohl NRDS weiterhin eine bedeutende Ursache für Morbidität und Mortalität ist.
Es wird geschätzt, dass etwa 50 Prozent der Todesfälle bei Neugeborenen an NRSD leiden.
Aufgrund der hohen Sterblichkeit sollten alle Neugeborenen-Intensivmediziner in der Lage sein, diese häufige Ursache für respiratorische Insuffizienz zu diagnostizieren und zu behandeln.
Alter des Beginns
Das Erkrankungsalter ist neonatal: Die Symptome und Anzeichen des Atemnotsyndroms treten beim Neugeborenen kurz nach der Geburt oder einige Minuten/Stunden nach der Geburt auf.
KINDERGESUNDHEIT: ERFAHREN SIE MEHR ÜBER MEDICHILD BEIM BESUCH DES STANDES AUF DER EMERGENCY EXPO
Ursachen: Tensidmangel
Der Säugling mit RDS leidet an Tensidmangel.
Surfactant (oder „Lungensurfactant“) ist eine Lipoproteinsubstanz, die von Typ-II-Pneumozyten auf alveolärer Ebene ab etwa der fünfunddreißigsten Schwangerschaftswoche produziert wird und deren Hauptfunktion darin besteht, die Oberflächenspannung zu verringern, indem sie die alveoläre Expansion während der Atmungsvorgänge garantiert: seine Abwesenheit ist daher begleitet von einer reduzierten alveolären Expansion und einer Tendenz zum Schließen mit beeinträchtigtem Gasaustausch, mit Beeinträchtigung der normalen Atmung.
Bei der Geburt muss Surfactant in ausreichender Menge und Qualität produziert werden, um einen endexspiratorischen Kollaps der Alveolen des Säuglings zu verhindern.
Verantwortlich für die Produktion dieses für die postnatale Lungenfunktion so wichtigen, tensidaktiven Materials sind die funktionell intakten alveolären Typ-II-Zellen (Typ-II-Pneumozyten).
Je früher ein Säugling ist, desto weniger verfügt er zum Zeitpunkt der Geburt über ausreichend Typ-II-Pneumozytenzellen und je früher er also ist, desto mehr fehlt ihm eine ausreichende Surfactant-Produktion.
Die Inzidenz von RDS bei Neugeborenen ist daher umgekehrt proportional zum Gestationsalter, und jedes Frühgeborene (Gestationsalter unter 38 Wochen) ist einem Risiko für diese Krankheit ausgesetzt.
Neugeborenes RDS hat eine hohe Prävalenz bei großen Frühgeborenen (Gestationsalter unter 29 Wochen) und Säuglingen mit niedrigem Geburtsgewicht (unter 1,500 Gramm).
Ein Mangel oder Fehlen des Tensids kann neben der Frühgeburtlichkeit verursacht oder begünstigt werden durch:
- Mutationen in einem oder mehreren Genen, die Surfactant-Proteine codieren;
- Mekoniumaspirationssyndrom;
- Sepsis.
Genetische Ursachen des neonatalen Atemnotsyndroms
Sehr seltene Fälle sind erblich und werden durch Mutationen in den Genen verursacht
- des Tensidproteins (SP-B und SP-C);
- des Adenosintriphosphat A3 (ABCA3)-Bindungskomplexes.
Ursachen: unreifes Lungenparenchym
Anfangs dachte man, das einzige Problem bei dieser Krankheit sei die verminderte Surfactant-Produktion der unreifen Lunge des Frühgeborenen, während neuere Studien gezeigt haben, dass das Problem sicherlich komplexer ist.
Tatsächlich hat das Frühgeborene nicht nur eine reduzierte Menge an Surfactant, sondern das vorhandene ist auch unreif und daher funktionell weniger effektiv.
Unklar ist auch, wie effektiv das Frühgeborene das vorhandene Surfactant verwerten kann.
Das Neugeborene mit RDS hat auch ein unreifes Lungenparenchym mit einer reduzierten alveolären Gasaustauschoberfläche, einer erhöhten Dicke der alveolar-kapillaren Membran, einem reduzierten pulmonalen Abwehrsystem, einer unreifen Brustwand und einer erhöhten Kapillarpermeabilität.
Jede akute Asphyxie-Episode oder reduzierte Lungenperfusion kann die Surfactant-Produktion stören, sie unzureichend machen und somit zur Pathogenese von RDS beitragen oder dessen Schweregrad erhöhen.
Risikofaktoren für neonatales RDS sind:
- Frühgeburt
- Gestationsalter von 28 Wochen oder weniger;
- niedriges Geburtsgewicht (weniger als 1500 Gramm, dh 1.5 kg)
- männliches Geschlecht;
- Kaukasische Rasse;
- diabetischer Vater;
- diabetische Mutter;
- Mutter standardmäßig unterernährt
- Mutter mit Mehrlingsschwangerschaften;
- Mutter missbraucht Alkohol und/oder nimmt Drogen;
- Mutter dem Rötelnvirus ausgesetzt;
- Kaiserschnitt ohne vorherige Wehen;
- Aspiration von Mekonium (das hauptsächlich bei Nach- oder Vollgeburten durch Kaiserschnitt auftritt);
- anhaltende pulmonale Hypertonie;
- vorübergehende Tachypnoe des Neugeborenen (neonatales Feuchtlungensyndrom);
- Bronchopulmonale Dysplasie;
- Geschwister, die zu früh und/oder mit Herzfehlbildungen geboren wurden.
Faktoren, die das Risiko für neonatales RDS (neonatale Atemnot) verringern, sind:
- fötale Wachstumsverzögerung
- Präeklampsie;
- Eklampsie;
- mütterlicher Bluthochdruck;
- längerer Membranbruch;
- Verwendung von Kortikosteroiden durch die Mutter.
Pathophysiologie
Alle Neugeborenen vollziehen ihren ersten Atemzug in dem Moment, in dem sie auf die Welt kommen.
Neugeborene müssen dazu einen hohen Lungendehnungsdruck ausüben, da die Lungen bei der Geburt vollständig kollabiert sind.
In normalen Situationen ermöglicht die Anwesenheit des Surfactants, dass die Oberflächenspannung in den Alveolen abnimmt, die Restfunktionsfähigkeit aufrechterhalten wird und folglich die Inspiration auf einem günstigen Niveau der Lungendruck-Volumen-Kurve beginnt: bei jedem Akt, der Die Restfunktionsfähigkeit nimmt zu, bis sie normale Werte erreicht.
Die abnorme Surfactant-Qualität und -Quantität führt beim kranken Kind zum Kollaps der Alveolarstrukturen und zu einer unregelmäßigen Verteilung der Ventilation.
Mit zunehmender Zahl kollabierender Alveolen ist der Säugling gezwungen, dynamische Kompensationsmechanismen auszuüben, um adäquat zu atmen, die darauf abzielen, den endexspiratorischen Druck zu erhöhen und so das Schließen der Alveolen zu verhindern:
- erhöht die Negativität des intrapleuralen Drucks während der Inspiration;
- hält die Atemmuskulatur beim Ausatmen tonisch aktiv, wodurch der Brustkorb steifer wird;
- erhöht den Atemwegswiderstand durch Adduktion der Stimmbänder beim Ausatmen;
- erhöht die Atemfrequenz und verkürzt die Exspirationszeit.
Die Dehnbarkeit der Brustwand, die während der Geburt von Vorteil ist, wenn der Fötus den utero-vaginalen Kanal passieren muss, kann ein Nachteil sein, wenn der RDS-Säugling inhaliert und versucht, die nicht dehnbaren Lungen auszudehnen, wie z Die Negativität des intrapleuralen Drucks, die bei dem Versuch, die nicht dehnbaren Lungen auszudehnen, erzeugt wird, nimmt zu, es gibt einen Zug zur Innenseite des Brustkorbs, und dieses Phänomen begrenzt die Lungenausdehnung.
Eine fortschreitende Lungenatelektase führt auch zu einer Verringerung des funktionellen Residualvolumens, was wiederum den Lungengasaustausch weiter verändert.
Daher werden hyaline Membranen gebildet, die aus einer durch Lungenschädigung produzierten Proteinsubstanz bestehen, die die Dehnbarkeit der Lunge weiter reduziert; Das Vorhandensein dieser Strukturen führt daher dazu, dass dieses pathologische Bild als "Hyaline Membran Disease" bezeichnet wird, ein Ausdruck, der in der Vergangenheit zur Bezeichnung dieses Syndroms verwendet wurde.
Die aus den geschädigten Alveolen austretende Proteinflüssigkeit bewirkt die Inaktivierung des knapp vorhandenen Tensids.
Das Vorhandensein dieser Flüssigkeit und eine sich verschlechternde Hypoxämie führen zur Bildung großer Bereiche von intrapulmonalen Shunts, die die Surfactant-Aktivität weiter hemmen.
So entsteht ein beängstigender Teufelskreis, der durch eine kontinuierliche Abfolge gekennzeichnet ist
- reduzierte Tensidproduktion
- Atelektase;
- reduzierte Lungendehnbarkeit;
- verändertes Verhältnis von Ventilation/Perfusion (V/P);
- Hypoxämie;
- weitere Reduzierung der Tensidproduktion
- Verschlechterung der Atelektase
Pathologische Anatomie
Makroskopisch erscheinen die Lungen von normaler Größe, sind aber kompakter, atelektatisch und haben eine purpurrote Farbe, die der der Leber ähnlicher ist. Sie sind auch schwerer als normal, so dass sie sinken, wenn sie in Wasser getaucht werden.
Mikroskopisch sind die Alveolen schlecht entwickelt und oft kollabiert.
Bei frühem Tod des Säuglings bemerkt man in den Bronchiolen und Alveolargängen Zelltrümmer, die durch die Nekrose der alveolären Pneumozyten verursacht werden, die bei erhöhter Überlebensrate von rosafarbenen hyaline Membranen umhüllt sind.
Diese Membranen bedecken die respiratorischen Bronchiolen, die Alveolargänge und seltener die Alveolen und bestehen aus Fibrinogen und Fibrin (sowie den oben beschriebenen nekrotischen Trümmern).
Das Vorhandensein einer schwachen Entzündungsreaktion kann ebenfalls festgestellt werden.
Das Vorhandensein von hyaline Membranen ist der typische Bestandteil einer pulmonalen hyaline Membranerkrankung, aber sie treten nicht bei Totgeburten oder Säuglingen auf, die nur wenige Stunden überleben.
Wenn der Säugling länger als 48 Stunden überlebt, treten reparative Phänomene auf: Proliferation des Alveolarepithels und Desquamation der Membranen, deren Fragmente sich in den Atemwegen verteilen, wo sie von Gewebemakrophagen verdaut oder phagozytiert werden.
Lesen Sie auch:
Obstruktive Schlafapnoe: Was es ist und wie man es behandelt
Obstruktive Schlafapnoe: Symptome und Behandlung der obstruktiven Schlafapnoe
Unser Atmungssystem: eine virtuelle Tour in unserem Körper
Klinische Bewertung: Akutes Atemnotsyndrom
Stress und Stress während der Schwangerschaft: So schützen Sie Mutter und Kind
Atemnot: Was sind die Anzeichen von Atemnot bei Neugeborenen?




