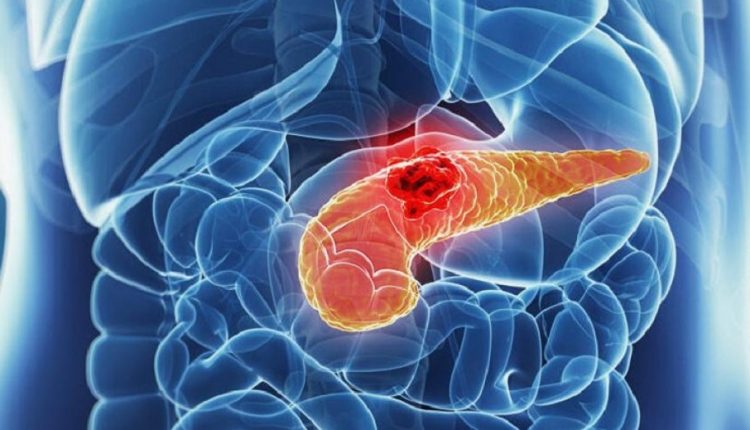
Pancréas : prévention et traitement du cancer du pancréas
Il existe plusieurs autres types de cancer du pancréas, mais l'adénocarcinome est la tumeur pancréatique la plus courante.
C'est une maladie qui trouve son origine dans les conduits qui transportent les enzymes digestives produites par le pancréas, dont les causes sont encore inconnues.
Il se forme à la suite de l'accumulation de cellules pancréatiques qui ont subi une altération génétique qui les fait se multiplier de manière incontrôlable, sans jamais mourir, et qui se développent et se propagent rapidement.
C'est pourquoi il s'agit d'une tumeur difficile à diagnostiquer à un stade précoce.
Types de tumeurs pancréatiques exocrines
Environ 80 % des tumeurs exocrines pancréatiques sont des adénocarcinomes de l'épithélium canalaire, et seulement 2 % sont bénignes.
Il existe des tumeurs exocrines très rares telles que le carcinome à cellules géantes, le carcinome adénosquameux, l'adénocarcinome microglandulaire, le carcinome mucineux, le cystadénocarcinome, le carcinome kystique papillaire, le cystadénocarcinome et le cystadénocarcinome à cellules acineuses et enfin le lymphome pancréatique primitif (tumeur débutant dans le tissu conjonctif).
Les tumeurs kystiques représentent moins de 5 % de toutes les tumeurs pancréatiques (cystadénomes et cystadénocarcinomes mucineux précoces), tandis que les tumeurs intracanalaires et mucineuses (bénignes et malignes) surviennent généralement sous la forme d'une dilatation kystique du système canalaire pancréatique.
Les tumeurs endocrines, qui sont initiées par les cellules du canal pancréatique, peuvent être fonctionnellement inactives, bénignes ou malignes et comprennent les insulinomes, les glucagonomes et les gastrinomes.
Environ 40 % des tumeurs endocrines pancréatiques ne sont pas fonctionnelles et jusqu'à 90 % d'entre elles sont malignes
Il existe plusieurs syndromes qui comprennent des néoplasmes associés à des tumeurs pancréatiques.
Parmi celles-ci, la plus connue est la néoplasie endocrinienne multiple (NEM) de type 1 (hyperplasie parathyroïdienne, tumeurs pancréatiques endocrines et tumeurs hypophysaires), et les gastrinomes et les insulinomes sont ici les plus fréquemment représentés.
Ces variations de la fonction tumorale influencent les stratégies de diagnostic et de traitement.
Stratégie clinique et traitement du cancer du pancréas
Lorsque le diagnostic de cancer du pancréas est posé, il est nécessaire d'évaluer s'il se prête à une résection chirurgicale radicale.
Une tumeur pancréatique en termes généraux est définie comme résécable lorsqu'elle peut être retirée sans laisser de résidu néoplasique (R0), non résécable lorsqu'elle ne peut pas être complètement réséquée (R1-2) ou borderline lorsque la radicalité est douteuse en préopératoire et qu'il faut s'appuyer sur des thérapies néoadjuvantes ou directement sur l'évaluation chirurgicale pendant la chirurgie.
Malheureusement, seulement environ 20 % des patients atteints d'un cancer du pancréas au moment du diagnostic sont radicalement résécables.
Par conséquent, il est crucial de définir le plus précisément possible le stade tumoral selon le système TNM (AJCC) pour éviter des interventions inutiles.
La stadification AJCC d'un cancer du pancréas est la suivante :
Tumeur (T)
TX - La tumeur primaire ne peut pas être évaluée
T0 - Aucune preuve de tumeur primaire
Tis – Carcinome in situ
T1 - Tumeur limitée au pancréas, 2 cm ou moins de taille maximale
T2 – Tumeur limitée au pancréas, supérieure à 2 cm dans sa plus grande dimension
T3 - La tumeur s'étend au-delà du pancréas (par exemple duodénum, voie biliaire, porte ou veine mésentérique supérieure) mais n'implique pas l'axe cœliaque ou l'artère mésentérique supérieure
T4 - La tumeur implique l'axe coeliaque ou les artères mésentériques supérieures
Ganglions lymphatiques régionaux (N)
NX - Les ganglions lymphatiques régionaux ne peuvent pas être évalués
N0 – Pas de métastases ganglionnaires régionales
N1 – Métastases ganglionnaires régionales
Métastases à distance (M)
MX – Les métastases à distance ne peuvent pas être évaluées
M0 – Pas de métastases à distance
M1 – Métastases à distance
Le groupement des stades du cancer du pancréas est le suivant :
Stade 0 – Tis, N0, M0
Stade IA – T1, N0, M0
Stade IB – T2, N0, M0
Stade IIA – T3, N0, M0
Stade IIB – T1-3, N1, M0
Stade III – T4, Tout N, M0
Stade IV – N'importe quel T, N'importe quel N, M1
Lors de la présentation initiale, seulement 20 % des patients ont une maladie de stade I, 40 % ont une maladie localement avancée et 40 % ont une maladie métastatique aux ganglions lymphatiques ou à des sites distants.
D'une manière générale, les stades T1 et T2 sont confinés au parenchyme pancréatique, tandis que les lésions T3 envahissent les structures locales telles que le duodénum, les voies biliaires et/ou les grandes veines péripancréatiques et les lésions T4 envahissent les organes environnants (par exemple, l'estomac, le côlon, le foie) ou les artères majeures. comme les artères mésentériques supérieures ou coeliaques.
Laparoscopie de stadification préopératoire
Certains centres préconisent d'effectuer une laparoscopie de mise en scène avant de procéder à la laparotomie.
Le but de la stadification laparoscopique est d'éviter de soumettre les patients présentant des métastases hépatiques ou péritonéales non visibles avec les méthodes radiologiques courantes à une chirurgie inutile.
Une telle enquête est cependant appropriée lorsque ces situations sont présentes :
- Niveau de CA 19-9 > 150 U/mL
- Ascite de faible volume
- Tumeurs dans le corps du pancréas
- Tumeurs borderline résécables
- Taille de la tumeur> 3 cm
- Lymphadénopathie des voies biliaires principales
- Thérapie et traitement du cancer du pancréas sous des formes opérables
Il existe un consensus raisonnable dans la littérature selon lequel la chirurgie, lorsqu'elle est radicalement possible, est la principale modalité de traitement du cancer du pancréas.
Cependant, il existe un rôle important pour la chimiothérapie et/ou la radiothérapie dans un contexte adjuvant ou néoadjuvant et dans le traitement des patients atteints d'une maladie non résécable.
Généralement, la maladie extrapancréatique exclut la résection curative et le traitement chirurgical peut être au mieux palliatif.
Généralement, l'infiltration vasculaire est considérée comme une contre-indication à la résection pancréatique, bien que de nos jours l'invasion de la veine porte mésentérique ou supérieure ne soit plus une contre-indication absolue, en fait cette dernière peut être retirée et reconstruite (de plus, dans de nombreux cas, la veine est seulement comprimée et non infiltré) en utilisant la veine jugulaire interne, la grande veine saphène ou la veine splénique.
Le bilan de l'infiltration des artères mésentériques supérieures, coeliaques et hépatiques est en revanche différent, car elles représentent incontestablement une contre-indication absolue à la résection radicale.
Dans ce contexte, l'approche chirurgicale doit être adaptée au site tumoral et donc une duodénocéphalopancréasectomie (DCP), avec ou sans pylore épargnant, une pancréasectomie totale (PT) et une pancréasectomie distale (PD) seront envisagées.
Ces interventions, qui nécessitent la réalisation de chirurgiens expérimentés dans ce type de chirurgie, présentent une incidence de complications et de risques préopératoires qu'il faut connaître et discuter avec le patient avant de procéder à l'intervention.
Les lignes directrices sur le cancer du pancréas de la Société européenne d'oncologie médicale (ESMO) indiquent que la résection chirurgicale complète est le seul traitement potentiellement curatif disponible ; cependant, la survie globale à 5 ans n'est que de 10 à 20 % et la survie à long terme chez les patients atteints d'une maladie propagée aux ganglions lymphatiques est extrêmement faible.
Les recommandations de l'ESMO incluent les éléments suivants
Le traitement symptomatique optimal joue un rôle clé dans la gestion de la maladie métastatique ; les patients peuvent avoir besoin d'un drainage ou d'un pontage en cas d'ictère obstructif ou d'obstruction gastrique.
La place de la chimiothérapie est limitée. La gemcitabine a été associée à un léger bénéfice de survie par rapport au bolus de 5-fluorouracile.
Chez les patients atteints d'un cancer du pancréas non résécable localement avancé, l'ablation locale a été explorée comme option thérapeutique. Une revue systématique a conclu que les stratégies suivantes semblent faisables et sûres :
- Ablation par radiofréquence (RFA)
- Électroporation irréversible
- Radiothérapie corporelle stéréotaxique (SBRT)
- Ultrasons focalisés de haute intensité (HIFU)
- Iode-125
- Iode-125-cryochirurgie
- La thérapie photodynamique
- Ablation par micro-ondes
- Il a été démontré que bon nombre de ces techniques ablatives soulagent la douleur et améliorent la survie.
Par exemple, une survie médiale allant jusqu'à 25.6 mois a été rapportée avec RFA et 24.0 mois avec SBRT. Des résultats prometteurs sur la qualité de vie ont été rapportés pour la SBRT.
Les autres procédures ont montré des résultats prometteurs dans certains établissements, mais ont encore une faible adoption.
Chimiothérapie du cancer du pancréas
Il n'existe actuellement aucun protocole de traitement qui donne des garanties de succès dans ce domaine.
On pense que chez les patients atteints d'une maladie métastatique, l'association de la gemcitabine et de l'erlotinib peut fournir une survie médiane et une survie à 1 an significativement plus élevées que l'utilisation de la gemcitabine seule.
Certaines études indiquent que l'association Gemcitabine-Capécitabine est l'une des options standard de première intention dans le cancer du pancréas localement avancé et métastatique, tandis que d'autres études ont montré que l'association FOLFIRINOX (leucovorine plus 5-lfuourouracil [LV5-FU] plus oxaliplatine plus irinotécan ) est capable de favoriser une survie médiane de 11.1 mois contre 6.8 mois dans le groupe Gemcitabine seule.
Il n'existe actuellement aucun protocole uniformément accepté et convenu.
Traitement adjuvant
Plusieurs études ont suggéré la possibilité que la chimiothérapie, avec ou sans radiothérapie, puisse améliorer de manière significative la survie médiane après résection chirurgicale d'une maladie opérable.
Ces études ne sont pas définitives et ne sont pas largement acceptées pour justifier un traitement par chimio-radiothérapie en traitement adjuvant.
Thérapie néoadjuvante
L'utilisation de la chimiothérapie et/ou de la radiothérapie dans le cadre néoadjuvant est également toujours source de controverse.
La justification de l'utilisation de la thérapie néoadjuvante comprend les affirmations suivantes :
- le cancer du pancréas est une maladie systémique et doit être traité systématiquement d'emblée ;
- les patients supportent mieux les effets toxiques de la chimiothérapie avant de subir ensuite une résection pancréatique majeure ;
- la taille de la tumeur peut diminuer avec le traitement néoadjuvant et la résection peut être moins complexe, conduisant à une meilleure survie globale.
Le problème est qu'il n'y a toujours pas d'accord définitif sur les protocoles de traitement à utiliser dans ce contexte clinique.
Duodénocéphalopancréasectomie (procédure DCP de Whipple)
Cette opération est réalisée chez des patients présentant une tumeur de la tête du pancréas, de la papille de Vater ou du cholédoque terminal ou du duodénum.
L'opération consiste traditionnellement en l'ablation de la tête pancréatique, du duodénum, de la vésicule biliaire et de l'antre de l'estomac, avec un drainage chirurgical du canal pancréatique distal et du système biliaire, généralement réalisé par anastomose avec une boucle digitale (anastomose biliaire-digestive).
Il a été démontré que le DCP a un taux de mortalité global de 6.6 % et un taux de morbidité de 25 %.
Les complications les plus graves sont les fistules anastomotiques, le retard gastrique et les hémorragies digestives.
Chez les patients présentant un ictère, de nombreux auteurs proposent l'utilisation d'un drainage biliaire (endoscopique ou transhépatique) mis en place en préopératoire.
Cependant, pour être efficace, le drainage biliaire doit être maintenu pendant un temps suffisant pour normaliser ou presque normaliser le taux de bilirubine (environ 20 jours).
Cependant, cette solution, en plus de retarder l'opération, prédispose au risque d'infection des voies biliaires, qui à son tour est associée à un risque accru de complications infectieuses postopératoires et d'infection de la plaie, et pour ces raisons ne trouve pas de partisans convaincus dans la majorité des auteurs.
L'opération standard de Whipple peut être modifiée en évitant la résection de l'antre gastrique en préservant le pylore.
Cette modification a été proposée pour améliorer l'état nutritionnel du patient (fonction réservoir de l'estomac), mais peut être grevée d'un risque accru de ralentissement de la vidange gastrique (ablation de l'innervation duodénale-gastrique).
D'un point de vue oncologique, il n'y a pas de différences entre les deux procédures.
Cancer du pancréas, les recommandations de la Société Européenne d'Oncologie Médicale donnent les recommandations suivantes
- la résection chirurgicale à intention radicale est le seul traitement potentiellement curatif disponible. Cependant, la survie globale à 5 ans n'est que de 10 à 20 % ; la survie à long terme dans les tumeurs avec des ganglions lymphatiques positifs est extrêmement faible.
- Le traitement symptomatique optimal joue un rôle clé dans la gestion de la maladie métastatique ; ces patients peuvent nécessiter un drainage ou une chirurgie de pontage pour ictère obstructif ou obstruction de la sortie gastrique.
- Le rôle de la chimiothérapie est limité ; La gemcitabine seule ou en association avec d'autres médicaments a été associée à un léger bénéfice de survie.
Pancréatectomie distale (PD)
Cette procédure a un taux de mortalité inférieur à la procédure standard de Whipple, à 3.5 %, mais son utilisation en résection curative reste limitée.
La PD est efficace et techniquement moins complexe que la DCP dans les tumeurs distales.
Malheureusement, les masses situées dans cette zone sont diagnostiquées beaucoup plus tard et sont donc généralement facilement inopérables en raison d'une thrombose vasculaire ou d'une infiltration gastrique ou intestinale.
La procédure implique l'isolement de la partie distale du pancréas contenant la tumeur, suivie de la résection de ce segment avec ou sans la rate, avec suture du canal pancréatique distal.
Les principales complications de la MP sont une fistule pancréatique, une hémorragie et un abcès.
Il est indispensable de placer des drains adéquats de la zone concernée par l'acte chirurgical.
Pancréasectomie totale (PT)
Bien que cette procédure soit la moins couramment pratiquée, elle peut néanmoins être un outil précieux dans le traitement chirurgical du cancer du pancréas, en particulier dans les cas où la tumeur implique le cou du pancréas ou si l'on soupçonne que la tumeur a métastasé le long du canal de Wirsung.
Le taux de mortalité est d'environ 8 % et la morbidité est plus faible (en effet, il n'y a pas de risque de fistules pancréatiques ou de déhiscence anastomotique), mais il en résulte un état définitif de diabète total postopératoire pas toujours facile à traiter.
Traitement palliatif du cancer du pancréas
Pain
Chez les patients qui ne se prêtent pas à une résection chirurgicale, il est nécessaire de proposer une thérapie pour prévenir et traiter les symptômes les plus importants et invalidants de la maladie.
Le soulagement de la douleur est crucial dans ce contexte.
L'utilisation d'antalgiques narcotiques doit être proposée précocement et à des dosages adaptés en association avec des antidépresseurs tricycliques ou des antiémétiques pour renforcer leurs effets antalgiques.
Chez les patients chez qui les narcotiques sont insuffisants, d'autres approches doivent être envisagées, telles que la neurolyse du ganglion coeliaque, qui peut apporter un soulagement significatif de la douleur à long terme.
Celle-ci peut être réalisée par voie transthoracique ou transabdominale en radiologie interventionnelle ou en anesthésie, trans-gastrique par injection à l'aiguille fine sous contrôle échographique ou scanner.
Soit en peropératoire lors de l'évaluation du potentiel de résection du patient.
La radiothérapie du cancer du pancréas peut soulager la douleur, mais elle n'affecte pas la survie du patient.
Certains patients peuvent ressentir des douleurs dues à une obstruction des voies pancréatiques ou biliaires, en particulier si la douleur s'aggrave considérablement après avoir mangé.
Ces patients peuvent bénéficier d'une décompression endoscopique avec drainage pancréatique placé par endoscopie rétrograde.
La jaunisse
L'ictère obstructif est une complication grave pour le patient atteint d'un cancer du pancréas de la tête, car il entraîne des démangeaisons intraitables, qui provoquent de graves lésions de grattage.
La résolution de ce symptôme peut être obtenue par la mise en place d'un drain biliaire interne (transtumoral) introduit par endoscopie rétrograde, interne externe (avec une branche externe et une branche transtumorale interne) ou externe (lorsque la tumeur n'est pas transitable) au moyen d'une voie transcutanée. procédure radiologique.
Les prothèses d'expansion en métal sont plus chères et permanentes, ont une période de perméabilité plus longue et sont préférables chez les patients dont l'espérance de vie est estimée à plus de 3 mois.
Ceux en plastique sont beaucoup moins chers et doivent généralement être remplacés tous les 3-4 mois et sont de préférence utilisés chez les patients ayant une espérance de vie plus courte.
Chez les patients en bon état général, ces interventions peuvent également être réalisées chirurgicalement, au moyen d'une anastomose bilio-digestive (pour contourner le néoplasme de la tête pancréatique), d'une anastomose gastro-digiunale pour éviter l'obstruction duodénale et assurer la continuité nutritionnelle, et d'une neurolyse cœliaque pour prévenir les douleurs pancréatiques.
Régime alimentaire pour les patients atteints d'un cancer du pancréas
Comme la plupart des patients atteints d'un cancer avancé, les patients atteints d'un cancer du pancréas sont souvent anorexiques.
La stimulation pharmacologique de l'appétit échoue généralement, mais peut être essayée.
Les patients peuvent présenter un certain degré de malabsorption secondaire à une insuffisance pancréatique exocrine causée par le cancer obstruant le canal pancréatique.
Les patients souffrant de diarrhée de malabsorption et de perte de poids peuvent bénéficier d'une supplémentation en enzymes pancréatiques.
Leur diarrhée peut également être améliorée en évitant les régimes riches en graisses ou en protéines.
Prévention du cancer du pancréas
Les données épidémiologiques montrent que le tabagisme est la cause d'environ 30 % des tumeurs pancréatiques.
Les carcinogènes spécifiques du tabac sont les méthylnitrosamines, les nitrosonornicotines, les hydrocarbures aromatiques polycycliques et les amines aromatiques.
Diverses études ont montré que les fumeurs de cigarettes développent un cancer du pancréas 3.3 à 9.5 ans plus tôt que les non-fumeurs.
Les fumeurs de cigarettes ont un risque 70% plus élevé de néoplasmes pancréatiques que les non-fumeurs.
Les cigarettes avec un filtre à fumée ne réduisent pas le risque de cancer.
Ne pas fumer ou arrêter définitivement de fumer doit être considéré comme un facteur important de prévention du cancer.
Les patients atteints de pancréatite chronique liée à l'alcool, s'ils fument depuis longtemps en même temps, ont également un risque accru de cancer du pancréas et de l'œsophage.
L'ablation chirurgicale du cancer du pancréas peut également avoir un aspect préventif chez les patients atteints de pancréatite alcoolique chronique.
Étant donné qu'environ 10 % de toutes les tumeurs pancréatiques se développent sur la base d'une pancréatite héréditaire chronique et d'une prédisposition génétique familiale, des examens de dépistage réguliers (EUS, scanner, IRM) tous les deux à quatre ans sont en cours de discussion pour ces groupes à risque à partir de 40 ans. .
Aucune preuve n'a encore été apportée quant à l'efficacité des examens de dépistage.
Cependant, l'expérience de l'utilisation de la résection prophylactique dans le cancer du pancréas à haut risque n'est à ce jour disponible que pour un petit nombre de patients.
Les patients atteints de néoplasmes kystiques du pancréas développent fréquemment un cancer du pancréas à long terme
Avec les tumeurs IPMN (Intraductal Papillary Mucinous Pancreatic Neoplasms), une transformation maligne en cancer canalaire du pancréas est observée chez environ 60 % à 70 % des patients.
Dans la néoplasie IPMN, le carcinome est principalement situé dans la tête du pancréas.
Les néoplasmes kystiques mucineux présentent une transformation maligne dans environ 20 % des cas.
Bien que la connaissance accrue des mutations génétiques séquentielles dans les néoplasies kystiques du pancréas ne permette pas encore une prédiction fiable du risque, l'expérience a montré que l'ablation chirurgicale est indiquée pour les néoplasies kystiques de plus de 2 ou 3 cm, surtout lorsque le diagnostic est connu (IPMN, MCN et adénome kystique séreux).
Dans nombre de ces maladies, l'ablation complète des néoplasmes kystiques est une stratégie de prévention du cancer et est désormais réalisée sans mortalité chirurgicale dans des centres spécialisés.
L'ablation complète d'une tumeur kystique (IPMN, MCN) offre aux patients un remède contre le néoplasme kystique et les soulage de la peur de développer un cancer du pancréas.
Lire aussi:
Diabète gestationnel, qu'est-ce que c'est et comment y faire face
Cancer du pancréas, une nouvelle approche pharmacologique pour réduire sa progression
Qu'est-ce que la pancréatite et quels sont les symptômes ?
Calculs rénaux : ce qu'ils sont, comment les traiter
Pancréatite aiguë : causes, symptômes, diagnostic et traitement



