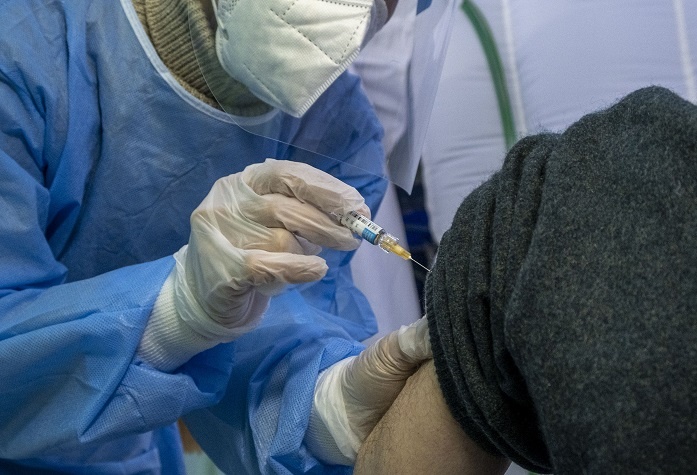
Covid, Agenzia europea per i medicinali (Ema): “Decisione su due vaccini entro il 29 dicembre e il 12 gennaio”
Covid, l’Agenzia europea per i farmaci (Ema) parla di vaccini: l’iter di approvazione riguarda i vaccini messi a punto da Pfizer-Biontech e Moderna
Ema ha reso noto che i due vaccini COVID-19 verranno commercializzati con l’inizio del 2021
L’Agenzia europea per i medicinali (Ema) ha reso noto che i due vaccini per il Covid-19 in fase di realizzazione da parte della società americana Pfizer insieme alla tedesca Biontech e da parte dell’americana Moderna potrebbero ricevere l’approvazione per la commercializzazione entro rispettivamente il 29 dicembre e il 12 gennaio.
Vaccini coronavirus commercializzati solo dopo valutazioni Ema
Secondo quanto comunicato dall’Ema, il Comitato per i medicinali per uso umano (Chmp), l’ente che si occupa di convalidare la commercializzazione di un farmaco, concludera’ le sue valutazioni sui vaccini in questione organizzando una riunione di emergenza “al massimo” entro le due date indicate.
La presidente della Commissione europea, Ursula von der Leyen, ha evidenziato oggi che i vaccini verrano autorizzati solo se risponderanno ai requisiti di “efficacia e sicurezza”.
Von der Leyen ha detto che la Commissione ha già “assicurato due miliardi di dosi” per i vaccini, evidenziando che gli Stati membri “stanno lavorando sui piani di vaccinazione e sulla logistica”.
Moderna ha affermato nei giorni scorsi che il suo vaccino ha terminato i test clinici, registrando un’efficacia del 94,1 per cento.
Risultato, questo, in linea con quello del 95 per cento annunciato da Pfizer e Biontech nei giorni scorsi.
Per approfondire:
Vaccino Covid in UE, la Commissione europea firma anche con CureVac



