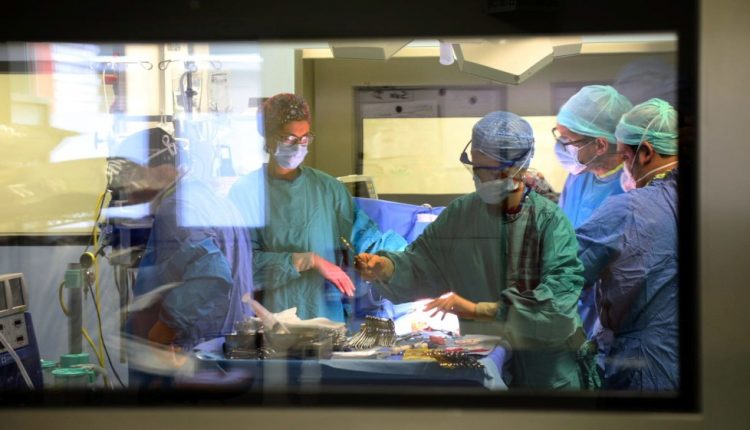
השתלת איברים: ממה היא מורכבת, מהם השלבים ומה צופן העתיד
השתלת איברים היא הליך כירורגי לפיו איבר חולה אחד או יותר (שתפקודם אינו ניתן להחלמה עוד) מוחלפים באיבר אחד או יותר שנלקח מתורם (גר או חי)
ניתוח ששורשיו, מבחינה רעיונית, בהיסטוריה הקדומה ביותר של האנושות (עליו דיברו לראשונה רופאים סינים), הוא בכל זאת פתרון טיפולי עדכני מאוד: הידע שאיפשר זאת (אימונולוגיה, חקר אנטיגנים...) נרכש רק בתחילת המאה ה-20.
משנת 1950 ואילך הפכה ההשתלה לבחירה מבוססת בטיפול באותן פתולוגיות המובילות להרס בלתי הפיך של האיבר, ולכן, למותו של החולה.
אבל השתלה היא לא רק הסיכוי האחרון למי שנשקפת סכנה לחייו: פעולה זו מאפשרת גם לשפר את איכות החיים של אותם חולים הסובלים ממחלות נכות כרוניות (למשל השתלת כליה לחולי דיאליזה).
עתיד ההשתלה עדיין לא משורטט, אבל ברור מאוד בתודעתם של מדענים ורופאים העוסקים במחקר: השתלת איברים מלאכותיים או איברים שנלקחו מבעלי חיים מהונדסים גנטית (קסנושתל), שיבוט והשתלה של תאי גזע הם רק חלק של הכיוונים שאליהם נע הנוף המדעי של העולם.
ניתוח השתלת איברים
המילה 'השתלה' מציינת פעמים רבות, באופן רדוקטיבי, את הפעולה של החלפת איבר חולה באיבר בריא.
במציאות, יש ארגון והיערכות שלמה מאחורי המבצע הזה הכולל דיוק וסנכרון קיצוני של אנשים ומכשירים.
תרגול הניתוח שונה בהתאם לתורם: אם הוצאת האיברים היא מאדם חי, למעשה, ניתן לתכנן את הניתוח; מה שכמובן אינו בר ביצוע אם האיברים מגיעים מתורם גופות, שמת מסיבות מקריות ובלתי צפויות.
לאחר שהוועדה הרפואית קיבלה את הסכמת המשפחה ומכריזה על מוות מוחי של התורם הפוטנציאלי, מתחילה הערכת הנתונים שלו: התאמה למקבלים פוטנציאליים ברשימות ההמתנה, היסטוריה רפואית, מאפיינים חיסוניים, קבוצת דם וכו'.
השתלת איברים מתפתחת בכמה שלבים
שלב 1
אדם עם פציעות שיכולות להיות תורם (למשל פגיעת ראש חמורה מאוד) מאושפז בטיפול נמרץ.
רופא מדבר עם המשפחה על האפשרות לתרום את איבריו; אם הם זמינים, מוקד התיאום מקבל התראה מיידית, האחראי לדיווח על התורם הפוטנציאלי וזיהוי הנמען הפוטנציאלי.
בינתיים, מוערכים נתוני המטופל התורם: התאמה למקבלים פוטנציאליים ברשימה, היסטוריה רפואית, מאפיינים חיסוניים. מתחילה תקופת התצפית של 6 שעות, שהיא חובה לפני האישור על מוות מוחי.
שלב 2
צוות ההסברים מופעל וחייב להיות זמין תוך זמן קצר מאוד.
הרופאים מגיעים לרוב למתקן במסוק. בתוך כך, בבית החולים בו תתבצע ההשתלה נקרא המושתל לעבור בדיקות שונות ולהעריך את מצב בריאותו.
כמו כן, מתבצעות בדיקות רבות לאיברים שייתרומו כדי למנוע העברת מחלות זיהומיות או גידולים מהתורם למקבל.
שלב 3
בתום תקופת התצפית, אם כל האינדיקציות מצביעות על אבחנה של מוות מוחי בלתי הפיך, ניתן להתחיל בהשתלה (כשעתיים).
המקבל נכנס לחדר הניתוח ומוכן לניתוח. מתן תרופות מדכאות חיסון מתחיל כעת כדי למנוע מהלימפוציטים לזהות את האיבר כזר ולגרום לדחייה.
שלב 4
לבסוף מגיע האיבר, שקוע בתמיסה מיוחדת להגנה על תאיו ומועבר במיכל מיוחד מלא בקרח כדי להאט את פעילותו התאית.
צוות רופאים אחד מכין את הנמען, השני דואג לנקות את האיבר המיועד להשתלה.
שלב 5
כעת ניתן להתחיל את ההשתלה: כלי הדם מחוברים, הדימום נשלט.
עבור לשלב 6
החולה יוצא מחדר הניתוח, אך עדיין נמצא בהרדמה, שתתארך לפחות עוד 6 עד 8 שעות כדי לאפשר לאיבר החדש להתרגל להפרש הטמפרטורות בין המיכל עם הקרח לגוף וכן, כמובן, לאיבר עצמו.
המטופל נשאר מחובר למכונה כדי לנשום.
עבור לשלב 7
החולה מתעורר ביחידה לטיפול נמרץ; אם מצבו הכללי טוב, מורידים אותו ממכשיר ההנשמה המלאכותית.
לאחר כ-4 ימים, הוא מתחיל שוב ללכת ולאכול.
לאחר כ-10 ימים הוא יוכל לעזוב את בית החולים ולחיות עם האיבר החדש שלו.
בתחילה, הוא יצטרך לחזור לבית החולים מדי יום לבדיקות אימונולוגיות; לאחר שנה, הוא יוכל לחזור אחת לחודשיים.
הסרת איברים
לאחר שהוכח מוות מוחי והשגת הסכמת המשפחה (במקרה של היעדר רצונות מפורשים של תורם), התורם הפוטנציאלי אינו נעזר עוד במכשיר ההנשמה המכאנית וניתן לאסוף את האיברים להשתלה באותו בית חולים שקבע התאמה .
הצוות שהוזעק בעבר נכנס לחדר הניתוח לצורך ניתוח ההסרה.
התנגדות להסרה אף פעם לא אומרת לעזור למטופל לקבל טיפול טוב יותר; הטיפול, למעשה, מסתיים ברגע שמתבסס מוות מוחי; התנגדות לכך משמעה רק שלילת חיים טובים יותר ממישהו אחר בזכות איבר חדש.
כיום צובר מקום גם סוג אחר של השתלות, זה מאנשים חיים.
ואכן, כיום ניתן לקחת אונת כליה, כבד או ריאה להשתלה אצל אנשים בסיכון במיוחד שלא ישרדו ברשימת ההמתנה.
לרוב מדובר בילדים, גם בגלל המחסור באיברים מושתלים בילדים וגם בגלל הגודל הקטן, מה שגם אומר שהתורם לא עומד בסיכון גבוה מדי.
לאחר שנלקחו, האיברים דורשים הליכים מיוחדים כדי לשמר אותם להשתלה.
לכל איבר יש זמן שימור מרבי, שמעבר לו הרקמות, שאינן מקבלות יותר דם, ולכן חמצן, נכנסות לנמק, כלומר התאים שלהן מתים, ולכן אינם ניתנים לשימוש.
זמנים אלו משתנים מאיבר לאיבר: לב (4-6 שעות), ריאה (4-6 שעות), כבד (12-18 שעות), כליה 48-72 שעות, לבלב (12-24 שעות).
השתלת איברים: דחייה
דחייה היא התגובה שיש לאורגניזם המקבל כלפי האיבר או הרקמה המושתלים.
למעשה, מערכת החיסון של הנמען מזהה את האיבר כזר ותוקפת אותו כאילו היה פתוגן.
ישנם ארבעה סוגי דחייה
- דחייה היפראקוטית: זו המהירה ביותר ומתרחשת תוך מספר דקות או שעות לאחר ההשתלה;
- דחייה מואצת: מתרחשת לעתים קרובות בחולים שכבר קיבלו השתלה קודמת ומתרחשת 3-4 ימים לאחר הניתוח;
- דחייה חריפה: מתרחשת לאחר פרק זמן שנע בין 5 ל-90 ימים; תסמינים ספציפיים הם בצקת, חום ואובדן תפקוד של האיבר המושתל;
- דחייה כרונית: מתפתחת כ-3 חודשים לאחר ההשתלה ועלולה לגרום לנזק לרקמות לאיבר החדש עד כדי אובדן תפקוד.
חווית דחייה של האיבר המושתל אינה אומרת בהכרח לאבד אותו באופן בלתי נמנע; להיפך, דחייה מטופלת בהצלחה אם ננקטת פעולה בתוך מסגרת זמן סבירה באמצעות שימוש בתרופות מדכאות חיסון.
המדכאים החיסוניים שהרופא רושם לאחר ההשתלה יסייעו לאיבר המושתל לא להסתכן בדחייה ולהישאר בריא.
מאחר שתאי מערכת החיסון שונים, גם התרופות שנקבעו לדיכוי חיסוני יהיו שונות.
אינדיקציות והתוויות נגד להשתלת איברים
האינדיקציה הגדולה והמיידית ביותר להשתלה היא כשל בלתי הפיך של איברים חיוניים כמו כליות, כבד, ריאות, לבלב, אך גם קרניות, מח עצם, מעיים.
ואכן, במקרים אלו, השתלה היא הטיפול היעיל היחיד להבטחת הישרדות.
לפיכך, כל מצב פתולוגי המונע מהאיבר לתפקד באופן שיאיים על הישרדות החולה, יש לראות באינדיקציה להשתלה.
טיפול לאחר הניתוח
לאחר ההשתלה מתקבלים בימים הראשונים במחלקה מצוידת לטיפול נמרץ, שם מתחילים טיפול מדכא חיסוני.
החולה המדוכא חיסוני דורש בידוד בחדרים 'סטריליים', שנוצרו במיוחד כדי למנוע זיהום מכל סוג שהוא מהסביבה החיצונית.
ה'קופסה' בה מתקבל לאחר פעולת ההשתלה מבודדת לחלוטין משאר יחידת ההחייאה המשמשת לניתוחים קונבנציונליים.
המצב של בידוד קפדני נמשך כל עוד נדרש למטופל להתגבר על השלב הקריטי שלאחר הניתוח (בדרך כלל 5-6 ימים), או במקרים בהם נדרש טיפול נגד דחייה.
ביקורים אצל חולים מושתלים
בתקופה המיידית שלאחר הניתוח מותרים ביקורים אצל קרובי משפחה קרובים כל עוד הם לבושים כראוי (על פי נוהלי הכניסה לחדר נקי).
כל אדם מתקבל לאזור הסינון בזה אחר זה וכמובן אסור להכניס אנשים עם חשד ו/או עדות למחלות זיהומיות.
התפתחויות עתידיות
הסוגיות החמורות ביותר ברפואת השתלות הן, מצד אחד, דחיית האיבר המושתל, ומצד שני, אי ספיקה של איברים שנתרמו בהשוואה לאלו הדרושים.
בשני הכיוונים, המחקר מתנסה בפתרונות שונים כדי להתגבר על בעיות אלו.
בכל הנוגע לדחייה, מנסים ליצור פתרונות המצליחים להערים על מערכת החיסון, ובכך להפחית את הטיפול המדכא את מערכת החיסון הנמצאת כיום בשימוש, או להגן על האיבר המושתל מפני התקפת לימפוציטים מסוג T, האחראים על סילוק חומרים מחוץ לגוף. .
בחזית השנייה, זו של מחסור באיברים, נערכים איברים מלאכותיים, הנדסת רקמות או השתלת קסנו שיכולים להחליף איברים אנושיים.
טיפול גנטי
באמצעות ריפוי גנטי ניתן להגיע למקור הבעיה ולהעלים פגמים גנטיים ישירות בתאים, ברקמות או באיברים הפגועים.
הגן הבריא מוכנס ישירות לנקודה הפגועה, שם הוא מתחיל לייצר את אותם חומרים שהגוף החולה אינו יכול לייצר בעצמו.
עם זאת, טיפול גנטי עדיין רחוק מלהיות בשימוש. על מנת להצליח להעביר דנ"א זר לגרעין התא, יש צורך ב'וקטורים' מיוחדים – וירוסים שאיבדו את תכונותיהם המדבקות, אך עדיין מסוגלים לתקוף תאים ולהעביר אליהם את המורשת הגנטית שלהם.
כדי להימנע מדחייה, האיבר שיושתל יצטרך לעבור טיפול במעבדה, תוך העברת גנים לתוכו שיאפשרו לו להגן על עצמו מפני המערכת החיסונית של הנמען.
כעת הגנים ידועים, אך עדיין לא מטפלים בהם בדיוק הדרוש. השלב הבא יהיה חיפוש אחר השילוב המושלם של הגנים המונע את פעולת כל המנגנונים האימונולוגיים של הנמען.
הנדסת רקמות
מטרת טיפול מסוג זה היא למצוא חלופה לאיברים אנושיים.
כבר כעת מצליחים החוקרים לייצר במעבדה רקמות כמו כלי דם, מסתמי לב, סחוס ועור.
ניתן היה להתגבר על הגבול החדש הזה הודות לעובדה שתאים נוטים להצטבר ליצירת איברים ורקמות.
תאי גזע
תאי גזע הם התאים הבלתי מובחנים שנמצאים בעוברים אנושיים שבוע לאחר ההפריה.
הם גם התאים ה'מתחילים' שמהם יתפתחו הרקמות והאיברים של הילד שייוולד.
תפקידם לווסת את התחלופה של תאי דם (תאי דם אדומים, תאי דם לבנים וטסיות דם) ואלו של מערכת החיסון (לימפוציטים).
כיום משתמשים במכונות ממוחשבות, מפרידות, לאיסוף תאים אלו, המאפשרות את בחירת התאים הדרושים. מקבלי התאים הם חולים הסובלים ממחלות עור, מחלות דם או גידולים מוצקים.
בנוסף לעובדה שתאי גזע עדיין לא ידועים במידה רבה, ישנה גם בעיה אתית: קצירת תאי גזע עובריים מרמזת על מותו של העובר.
לכן הדרך לקצור תאי גזע ממבוגרים משתכללת.
שיבוט
טכניקת השיבוט תאפשר לעקוף לחלוטין את בעיית דחיית האיברים.
זה יהיה כרוך בהחדרת גרעין התא של החולה, עם כל המורשת הגנטית שלו, לתוך תא גזע של עובר אנושי או ביצית שקודם לכן לא היה לו גרעין משלו.
תאים מעובדים אלה, שיטופחו במבחנה במעבדה, יהיו זהים גנטית לאלו של מערכת החיסון של המטופל, שלא תזהה אותם כזרים.
טכניקה זו אינה אופציה מעשית כיום מכיוון שגם שיבוט, קציר תאי גזע וגם שימוש חסר הבחנה בביציות אסורים על פי חוק.
השתלת קסנו
נראה כי השתלת קסנו, כלומר השתלת תאים, רקמות ואיברים של בעלי חיים בבני אדם, היא הפתרון העתידי למחסור באיברים להשתלה.
הניסויים בתחום זה הם רבים ומתמודדים עם בעיות אתיות, פסיכולוגיות ואחרון חביב, חיסוניות.
הניסיונות המעטים שנעשו, למעשה (כבד חזיר ולב בבון שהושתלו בשני בני אדם שונים) לא הניבו את התוצאות הרצויות.
משבר הדחייה, למעשה, היה אלים במיוחד ובלתי אפשרי לשלוט בו.
אולם הטכניקה הזו יכולה להיות באמת הפתרון למחסור באיברים.
למעשה, מה שהכי חוששים ממנו הוא התפתחות של זיהומים טיפוסיים של בעלי חיים, המועברים לבני אדם באמצעות פתוגנים הנמצאים באיבר המיועד להשתלה, שעלולים להיות הרות אסון.
חלופה אפשרית לנכות זו יכולה להיות שינויים גנטיים בחיות תורמות; בפועל, החיות יגדלו בסביבה סטרילית ויעברו שינויים גנטית כדי להפוך את איבריהן למתאימים יותר לאורגניזם של הנמען.
עם זאת, לעת עתה, הושגו כמה אבני דרך; אלו הן השתלות קסנו של תאים ולא השתלות קסנו של איברים, כגון תאי עוברי חזירים לטיפול במחלת פרקינסון, תאי מח בבון שהושתלו בחולי איידס סופניים בניסיון לשחזר את מערכת החיסון של החולים, או אינסולות לבלב שעדיין מחזירים בגירוי של ייצור אינסולין כטיפול נגד סוכרת.
השתלת איברים: איברים מלאכותיים
פתרון נוסף לאי ספיקת איברים כמו דחייה הוא איברים מלאכותיים.
הבעיה העיקרית היא תאימות ביולוגית; אלו הם, אחרי הכל, איברים מכניים שצריכים להסתגל לאורגניזם ביולוגי.
התאימות הביולוגית חייבת לכסות את כל המאפיינים המורפולוגיים, הפיזיקליים, הכימיים והתפקודיים המסוגלים לספק את הפונקציונליות של האיבר ובמקביל, את הישרדותו ללא סיכון של דחייה.
כל ההשלכות הללו הן שהופכות את ייצורם של איברים מלאכותיים המסוגלים להחליף באופן מלא ומושלם איברים 'טבעיים' בתפקודם למורכב.
קרא גם:
השתלת איברים: אבחון וטיפול בחולים הממתינים
הנחיות ראשונות לשימוש ב-ECMO בחולים ילדים העוברים השתלת תאי גזע המטופואטיים
כיצד מתבצעת השתלת פנים? - וידאו
AI מציל לב: מערכת בינה מלאכותית מראה הבטחה בזיהוי סימנים של דחיית השתלות לב
אי ספיקת לב ואינטליגנציה מלאכותית: אלגוריתם למידה עצמית לזיהוי סימנים בלתי נראים לא.ק.ג.



