Ģimenes hiperholesterinēmija: kas tas ir un kā to ārstēt
Ģimenes hiperholesterinēmija, reta ģenētiska slimība, kas izraisa nopietnas sekas veselībai (piemēram, sirdslēkme un insults), kurai nepieciešami atbilstoši ierobežošanas pasākumi ar atbilstošām zālēm un atbilstošu dzīvesveidu.
Ko nozīmē hiperholesterinēmija? Un ko nozīmē ģimenes?
Hiperholesterinēmija ir klīnisks stāvoklis, kam raksturīgs pārmērīgs holesterīna līmenis asinīs.
Holesterīns ir lipīdu sastāvdaļa, ko parasti lieto kopā ar uzturu, bet ko var ražot arī organisms.
Holesterīns ir ļoti svarīgs dzīvei, jo to izmanto šūnu membrānu veidošanai (lai nodrošinātu to darbību), aizsargā neironus un galvaskausa nervus.
Holesterīnu lieto arī citu molekulu sintēzei, no kurām trīs ir žultsskābes (svarīgas gremošanai), daži hormoni un D vitamīns.
Tikai tad, ja tas pārsniedz šīs prasības, tas var radīt nopietnus zaudējumus.
Hiperholesterinēmijas gadījumā holesterīns asinīs uzkrājas vieglu lipoproteīnu (ZBL), konkrētu tauku un olbaltumvielu agregātu veidā, kurus dēvē arī par “slikto holesterīnu” un kas veicina plāksnes veidošanos artērijas sieniņā (aterosklerozes plāksnes).
Tas notiek, ja pacientiem ir tik augsts holesterīna līmenis, ka viņi to nevar novērst, izmantojot aknu fizioloģiskos mehānismus.
ZBL uzkrāšanās asinīs galu galā noved pie ateromas (fiziskas obstrukcijas normālai asins plūsmai) veidošanās, kas var izraisīt nopietnākas sekas, piemēram, stenokardiju, sirdslēkmi, insultu, bet arī citos orgānos, piemēram, smadzenēs, nieres, plaušas un pašas aknas.
Hiperholesterinēmija ir pazīstama, ja to pārnēsā pēcnācējiem
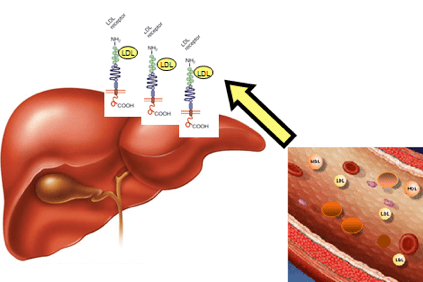
Tas ir saistīts ar gēna modifikācijām, kas satur informāciju, lai iegūtu aknu olbaltumvielu - ZBLR (ZBLR) receptoru, kas atpazīst ZBL, izved to no asinsrites un transportē uz aknu šūnām, kas pēc tam to noņem. Šīs gēnu izmaiņas izraisa ZBL uzkrāšanos asinīs.
Līdz šim ZBL gēnā ir zināmas vairāk nekā 600 izmaiņas, kas izraisa ģimenes hiperholesterinēmiju.
Arī cilvēki ar šo traucējumu var izraisīt izmaiņas citos gēnos, kas iesaistīti lipoproteīnu metabolismā, piemēram, APOB gēns (apoproteīns B ZBL) un PCSK9 gēns (olbaltumviela, kas noārda ZBL receptorus).
Lai gan ir zināms, ka holesterīna uzkrāšanās var būt kaitīga, tiek lēsts, ka līdz vienai trešdaļai sirdslēkmes, kas radušās pirms 40 gadu vecuma, cēlonis ir nediagnosticēta vai neatbilstoši ārstēta ģimenes hiperholesterinēmija.
Biežāk sastopama daudzfaktoru hiperholesterinēmija, ko izraisa vides faktori (diēta ar augstu tauku saturu, īpaši, ja tā saistīta ar fizisku neaktivitāti) pat predisponējošu ģenētisko faktoru klātbūtnē.
Ģimenes hiperholesterinēmijas izpausmes formas
Šī slimība var izpausties divās dažādās formās: mazāk nopietna (heterozigota, 2 gadījums uz 1 indivīdiem) un nopietnāka (homozigota, 500 gadījums uz 1 1,000,000 1,2 indivīdu) XNUMX.
Heterozigotiskā forma bieži ir asimptomātiska un tiek diagnosticēta tikai, pamatojoties uz holesterīna līmeni asinīs.
Aknas cenšas novērst ZBL, jo ZBL receptori tiek ražoti nepietiekamā skaitā, kā rezultātā 2 vai 3 reizes palielinās asins līmenis salīdzinājumā ar normālām vērtībām.
Šī forma var izraisīt paaugstinātu sirds un asinsvadu slimību risku pieaugušā vecumā.
Homozigotu formu raksturo sirds un asinsvadu slimību rašanās pat jaunā vecumā un raksturīgu tauku uzkrāšanās klātbūtne, piemēram, ksantomas (dzeltenīgi mezgliņi uz roku un Ahileja cīpslas) un ksantelasma (dzeltenīgas plāksnes uz plakstiņiem un ap to). acis).
Ģenētiskais defekts tiek mantots no abiem vecākiem, un sirdslēkmes risks terapijas neesamības gadījumā jau tiek novērots apmēram 15-20 gadu vecumā.
Faktiski šajā stāvoklī aknas nespēj metabolizēt asinīs palikušos lipoproteīnus, kas pēc tam uzkrājas, izraisot iepriekš aprakstītās disfunkcijas un radot situāciju, kas nav saderīga ar dzīvi.
Kādas ir slimības pārnešanas iespējas bērniem?
Tā kā katram no mums ir divas katra gēna kopijas, kuras katra ir mantojusi no vecākiem, mums būs heterozigota forma, kad mēs mantosim vienu izmainītu un vienu veselīgu kopiju.
Tieši pretēji, mums būs homozigota forma, ja mēs no abiem vecākiem mantosim abas slimā gēna kopijas. Jāsaka, ka šī forma ir ļoti reta, jo tā notiek tikai tad, ja abiem vecākiem ir gēns, kas izraisa šo slimību, un tāpēc katrs no viņiem var pārsūtīt vienas un tās pašas gēnu izmaiņas kopiju.
Ģimenes hiperholesterinēmiju sauc par heterozigotu patoloģiju, kas sastāv retos gadījumos, kad tiek mantoti divu dažādu veidu gēnu pārveidojumi, pa vienam no vecākiem.
Bērni, kuriem ir risks saslimt ar šo slimību, ir savlaicīgi jānosaka un jāārstē. Šodien slimību ir iespējams diagnosticēt, izmantojot ģenētiskos testus, kas meklē kļūdas (gēnu izmaiņas) uz LDLR, ApoB un PCSK9 gēniem.
Tāpēc ir pārnēsājamas tikai ģimenes hiperholesterinēmijas formas.
Tomēr daudzfaktoru formas, kas rodas galvenokārt nepareiza dzīvesveida dēļ (holesterīna uzkrāšanās ar uzturu), var raksturot arī ar ģenētisku noslieci.
Faktiski šiem priekšmetiem var būt ģenētisks deficīts, kas apdraud ķermeņa spēju pienācīgi kompensēt lipīdu pārpalikumu uzturā.
Piemēram, kad aknas ir piesātinātas ar holesterīnu, kas uzņemts kopā ar pārtiku, var tikt nomākta tādu receptoru ražošana, kas uztver asinīs cirkulējošo ZBL.
Situācija ir ļoti līdzīga tai, kāda rodas ģimenes hiperholesterinēmijas laikā, kaut arī tā nav tik smaga.
Šajā gadījumā kopējā holesterīna koncentrācija asinīs pārsniedz normu un parasti ir robežās no 240 līdz 350 mg / dl, salīdzinot ar normālo, kuru parasti nosaka ap 200 - 240 mg / dl.
Kuriozs: šī slimība, iespējams, ir nodota gadsimtu garumā
Uzmanīgs slavenās Monas Lizas gleznas novērojums parāda iespēju, ka Mona Liza jau jaunībā cieta no ģimenes hiperholesterinēmijas.
Patiesībā Leonardo arī uzticīgi attēlo tipiskos tauku nogulsnes uz rokām un acu tuvumā (tagad pazīstamas kā ksantomas un ksantelasmas), kas droši norāda uz patoloģijas klātbūtni.
Ja tā ir taisnība, tiek parādīts, ka ģimenes hiperholesterinēmija ir gadsimtiem ilgi saglabājusies slimība (gadījums, kas dokumentēts jau 1500. gadā).
Kādas ir iespējas šodien ārstēt šo slimību?
Slimības izārstēšanas iespēja ir atkarīga no tās smaguma pakāpes. Arī riska faktori (diēta, smēķēšana, vecums, ģimene un hiperholesterinēmijas personīgā vēsture, citu slimību klātbūtne) var pasliktināt kopējo slimības ainu.
Ģimenes hiperholesterinēmijas ārstēšanai var izmantot jaunās paaudzes zāles, taču tajā pašā laikā ir jārīkojas ar atbilstošu dzīvesveida modifikāciju.
Vidējas smaguma pakāpes (ģimenes heterozigotu hiperholesterinēmija) gadījumā uz statīnu balstīta zāļu terapija (holesterīna sintēzes inhibitori, kas izraisa paaugstinātu ZBLR receptoru sintēzi) un kombinācija ar ezetimibu (holesterīna absorbcijas inhibitori) vai PCSK9 inhibitoriem (ti, PCSK9 olbaltumvielu inhibitoriem, kuru loma ir iznīcina aknu receptorus, kas uztver ZBLR) uzlabo ZBLR gēna veselīgās kopijas aktivitāti un samazina holesterīna uzkrāšanos asinīs.
Nesen apstiprināta ir arī bempedoskābe, zāles, kas darbojas aknās, inhibējot enzīmu ATP citrāta liāzi - molekulu, kas iesaistīta endogēnā holesterīna sintēzes procesā.
Šis darbības mehānisms ļauj mums iedarboties uz saražotā holesterīna daudzumu, kas darbojas augšpus straumes no statīnu darbības vietas, un stimulēt ZBL receptoru izpausmi, lai kompensētu samazināto sintēzi.
Atšķirībā no statīniem, bempedoskābe skeleta muskuļos nav aktīva, kas samazina statīniem raksturīgu nevēlamu notikumu iespējamību.
Šīs zāles var saistīt arī ar ezetimibu ar labvēlīgu iedarbību.
Homozigota ģimenes hiperholesterinēmija vēl nesen tika uzskatīta par neārstējamu slimību.
Terapija, kuras pamatā ir statīni, šajā patoloģijā nav efektīva. Faktiski statīni, kas iedarbojas uz mehānismiem, kas izraisa endogēna holesterīna ražošanu, nevar stimulēt ZBL receptoru sintēzi.
Lai ZBL holesterīnu izvadītu no šo pacientu ķermeņa, plazmaferēze, metode, kas ļauj filtrēt asinis, izvadot taukus, līdzīgi kā to dara ar dialīzi, kad nieres nedarbojas.
Tomēr šī ir invazīva procedūra, kas negatīvi ietekmē pacientu dzīves kvalitāti.
Jaunākie pētījumi par ģimenes hiperholesterinēmiju
Pēdējo gadu laikā pētījumi ir noveduši pie specifisku zāļu izstrādes arī ģimenes hiperholesterinēmijas homozigotajai formai, ievērojami uzlabojot ar to slimo pacientu gaidas un dzīves kvalitāti.
Piemēram, zāļu lomitapīds (iekšķīgi lietots) šiem pacientiem ievērojami samazina ZBL holesterīna līmeni plazmā.
Lomitapīds nomāc mikrosomu triglicerīdu transporta olbaltumvielu (MTP), kas ļauj šos lipīdus kopā ar apoproteīnu B100 iestrādāt topošajos VLDL.
Rezultātā apoproteīnu B100 un ZBL daudzums samazinās pat pacientiem, ja slimība ir izraisījusi ZBL receptoru pilnīgu neesamību.
Vēl viena jaunās paaudzes zāles ir mipomersēns, antisense oligonukleotīds, kas spēj noārdīt B100 apoproteīnus, kas piedalās ZBL veidošanā, tādējādi samazinot pēdējo skaitu.
Evolokumabs un alirokumabs ir divas monoklonālas antivielas, kas inhibē PCSK9 olbaltumvielu aktivitāti asinīs.
Tomēr, lai šīs divas zāles iedarbotos, vismaz nelielai daļai ZBL receptoru jābūt klāt un jādarbojas.
Starp zālēm, kas joprojām ir klīniskās attīstības stadijā, ir iekļauta bioloģiska zāle (tā sauktā siRNS), kas bloķē DNS transkripciju un PCSK9 olbaltumvielu sintēzi aknās.
Nesen ir sasniegti pozitīvi rezultāti ar evinacumabu, kas ir olbaltumvielu līdzīga angiopoetīna 3 monoklonālu antivielu inhibitors (ANGPTL3) - molekula, ko sintezē aknas un kuras uzdevums ir palielināt holesterīna-LLDL un triglicerīdu līmeni, novēršot to noārdīšanos.
Šīs jaunās zāles ir parādījušas efektivitāti arī pacientiem, kuriem ZBL receptori nedarbojas3,4.
Nesen ir veikti arī daži mēģinājumi saprast, vai gēnu terapija, ieviešot veselīgo gēnu pacienta DNS, varētu darboties5.
No šī ģimenes hiperholesterinēmijas iespējamo terapiju saraksta ir iespējams saprast, cik daudz pētījumu veic, lai piedāvātu risinājumus šiem pacientiem, kuri, lai arī reti, tomēr cieš no šīs smagās slimības, samazinot letālu seku risku.
Tomēr, kā tas vienmēr notiek ar jaunām zālēm, ir ieteicams lietot piesardzības vārdu par to hronisku lietošanu, jo zināšanas par to iespējamām blakusparādībām būs skaidrākas tikai ar pieredzi (farmakovigilance), tāpēc rūpīgi jāizvērtē to lietošana pediatrijā, protams, ar galveno mērķi piedāvāt šiem “mazajiem” pacientiem iespēju dzīvot “normālu” dzīvi.
Bibliogrāfiskas un sitogrāfiskas atsauces uz rakstu par ģimenes hiperholesterinēmiju
1 2019. gada ESC / EAS vadlīnijas dislipidēmiju ārstēšanai: lipīdu modifikācija kardiovaskulārā riska mazināšanai. Autori / darba grupas locekļi; ESK Praktisko vadlīniju komiteja (CPG); ESC Nacionālās sirds biedrības. Ateroskleroze. 2019. gada novembris; 290: 140–205. doi: 10.1016 / j.atherosclerosis.2019.08.014.
2 Retas dislipidēmijas, sākot no fenotipa līdz genotipam un beidzot ar vadību: Eiropas Aterosklerozes biedrības darba grupas vienprātības paziņojums. Hegele RA, Borén J, Ginsberg HN, Arca M, Averna M, Binder CJ, Calabresi L, Chapman MJ, Cuchel M, von Eckardstein A, Frikke-Schmidt R, Gaudet D, Hovingh GK, Kronenberg F, Lütjohann D, Parhofer KG , Raal FJ, Ray KK, Remaley AT, Stock JK, Stroes ES, Tokgözoğlu L, Catapano AL. Lancet diabēta endokrinols. 2020. gada janvāris; 8 (1): 50–67. doi: 10.1016 / S2213-8587 (19) 30264-5.
3 Lipoproteīni (a) Lipoproteīnu aferēzes samazināšana līdz Antisense oligonukleotīdu pieejai. Greco MF, Sirtori CR, Corsini A, Ezhov M, Sampietro T, Ruscica MJ Clin Med. 2020. gada 3. jūlijs; 9 (7): 2103. doi: 10.3390 / jcm9072103.
4 ZBL holesterīna līmeni pazeminošā terapija. Pirillo A, Norata GD, Catapano AL. Handb Exp Pharmacol. 2020. gada 30. aprīlis. Doi: 10.1007 / 164_2020_361.
5 Ģimenes hiperholesterinēmijas gēnu un šūnu terapijas pārskats. Hajighasemi S, Mahdavi Gorabi A, Bianconi V, Pirro M, Banach M, Ahmadi Tafti H, Reiner Ž, Sahebkar A. Pharmacol Res. 2019. gada maijs; 143: 119-132. doi: 10.1016 / j.phrs.2019.03.016.



