Teste de acordo com COVID-19, as indicações do Ministro da Salute ai medici italiani: ecco quali usare e perché
Teste por COVID-19, il Ministero della Salute ha diffuso il documento “Test di laboratorio per SARS-CoV-2 and loro use in sanità pubblica”, contente indicazioni sui criteri di scelta dei test a disposizione, per un use razionale e sostenibile delle risorse nei diversi contesti.
E 'il documento di riferimento per i medici italiani, e viene diffuso in Pdf da Fnomceo, la Federazione degli Ordini dei Medici e degli Odontoiatri italiani.
Perché nel mezzo della seconda ondata dell'epidemia di coronavirus, è essenziale la scelta dei test a disposizione nei diversi contesti per un use razionale e sostenibile delle risorse.
Este documento riassume as informações disponíveis no momento da sua publicação e pode ser aggiornato se ulteriori evidenze scientifiche saranno disponível.
Teste COVID-19, os indicadores da OMS
As indicações neste documento estão em linha com as indicações na Organização Mundial da Saúde (OMS) para o perfil dos produtos por diagnóstica che hanno como alvo COVID-19, assim como chegar riportati no documento “Perfis de produtos alvo para diagnósticos prioritários para apoiar a resposta a a pandemia COVID19 v.1.0 ”de 28 de setembro de 2020 que descreve as características principais do teste por SARS-CoV-2, ma che sottolineano anche la necessità che essi soddisfino non solo i criteri di specificità e sensibilità, ma anche caratteristiche di test rapido che ne favorisca l'uso in determinati contesti.
Centro Europeu de Prevenção e Controle de Doenças (ECDC) riconosce 5 obiettivi per il testing: controllare la trasmissione;
monitorare l'incidenza, l'andamento e valutare la gravità nel tempo;
mitigare l'impatto del COVID-19 nelle strutture sanitarie e socioassistenziali;
nivelar cluster ou focolai em concursos específicos;
Prevenir a (re) introdução de qualquer área que hanno raggiunto ao controle de segurança do vírus.
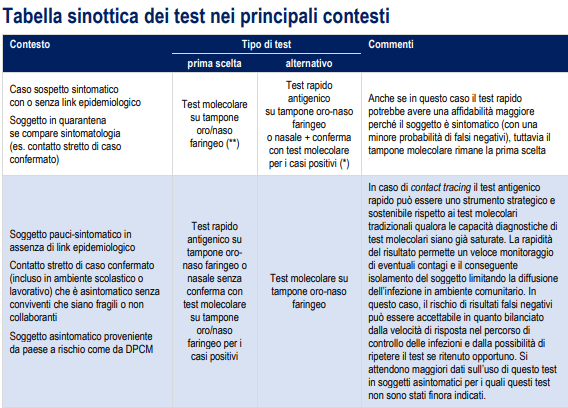
Eu testo o COVID-19 atualmente disponível para o scopi di sanità pubblica
Actualmente i test possono essere suddivisi in tre grandi gruppi: tampone molecolare, tampone antigenico rapido, test sierologici.
COVID-19, il test molecolare por tamponamento
Transcrição reversa molecular (rt) -Real Time PCR para a recuperação do genoma (RNA) do vírus SARS-CoV-2 no campo biológico.
Esta metodologia permite identificar em modo altamente específico e sensível um ou mais geni bersaglio del vírus presente no campione biológico e di misurare in tempo real la concentrazione iniziale della sequenza target.
I saggi in rt-Real Time PCR, seppur con indicazioni qualitativo, pois vem descritti and suggeriti dagli organi internazionali di riferimento, permettono di ottenere una curva di amplificazione il cui Cycle Threshold o ciclo soglia (CT) é inversamente proporcionale alla quantità del bersaglio genico stampo iniziale presente nel campione.
Quindi, em base a questo principio, maggiore è il numero delle “molecular stampo” presenti all'inizio della reazione e minore sarà il numero di cicli necessari per raggiungere un determinato valore di CT.
Viceversa, un alto valore di CT, ottenuto dopo numerosi cicli di amplificazione, indica una bassa quantità di target genico iniziale e quindi di genoma virale. O PCR em tempo real é o “padrão ouro” de acordo com os diagnósticos do COVID-19.
La rilevazione dell'RNA virale di SARS-CoV-2 eseguita in laboratorio da campioni clinici (in genere tamponi nasofaringei o orofaringei) e oggi rimane il saggio di riferimento internazionale per sensibilità e specificità ed è in grado di rilevare il patogénica virale in soggetti sintomatici, pre-sintomatici o asintomatici.
Para a complessità della metodica, la rilevazione di SARS-CoV-2 viene esclusivamente in laboratori specializzati con operatori esperti (5).
Il risultato può esser ottenuto in un minimo di 3-5 ore ma situazioni organizzative and logistiche possono richiedere anche 1-2 giorni.
È necessario ricordare che ai fini della segnalazione dei casi nel sistema della sorveglianza integrata COVID-19, coordinata da ISS, vengono considerati solo i risultati positivi ottenuti tramite rt-PCR em tempo real dai laboratori di riferizzati regionali ou dai laboratori identificati / autori de questi https://www.epicentro.iss.it/coronavirus/sars-cov-2- sorveglianza).
Sim aggiunge la possibilità di effettuare l'analisi dei test molecolari senza effettuare l'estrazione and la purificazione dell'RNA dal campione biologico, pode utilizar la tecnica della inattivazione al calore (95 ° C / 98 ° C) ("a crudo" )
Ciò permette di semplificare, massimizzare e velocizzare il primo step dell'analisi stessa, specialmente in condizioni di forte pressione sui laboratori dovuti all'aumentare dei tamponi da processare.
Il rischio di perdita di sensibilità può considerarsi minimo and present only ad Alti numeri di cicli di amplificazione della PCR, come riportato of lavori scientifici internazionali (6-7).
Tuttavia, a sensibilidade resulta ser superior ao teste antigênico.
Teste antigenico rápido (mediante tampone nasale, naso-oro-faringeo, salivare) por il Covid-19
Negli ultimi mesi, sleep stati sviluppati nuovi tipi di test che promettono di offrire risultati mais rapidamente (30-60 minuti), con menor custo e senza la necessità di personale specializzato (8).
Essas perguntas foram feitas para testar os antígenos rápidos, os instrumentos potencialmente úteis para soprar para os indivíduos de triagem.
Analogamente ai test molecolari, i saggi antigenici are di type directto, ossia valutano directtamente la presenza del virus nel campione clinico, a diffenza dei test sierologici che son di type indiretto, cio rilevano la presenza di colorrpi specifici che indicano una infezione pregressa o in atto .
Um teste diferencial molecular, però, i test antigenici rilevano la presenza del virus non tramite il suo ácido nucleico ma tramite le sue proteine (antigeni).
Este teste contém o substrato anticorrospi specifici in grado di legarsi agli antigeni virali di SARS-CoV-2 ed il risultato della reazione antigen-anticorpo può essere direttamente visibile a occhio nudo ou letto mediante um simples aparelho semplice al "point of care" senza la necessità di essere effettuato in un laboratorio.
Os antígenos de teste de Negli Stati Uniti 3 rápidos foram aprovados pela FDA. Na Europa, numerosi test hanno già ottenuto il Marca CE e diversas aziende di diagnostica stanno lavorando per ottenere l'approvazione normativa idonea per essere immessi sul mercato con un sufficiente grado di affidabilità (9).
Eu testo antigenici sono di tipo qualitativo (sim / no) e intercetano, tramite anticorrospi policlonali ou monoclonali, specifici peptidi (porzioni proteiche) della proteina S (Spike) o N (nucleocapsídeo) presenti sulla superficie virale di SARS-CoV-2.
O teste pode resultar negativo se a concentração de gli antigeni é inferiore al limite de rilevamento do teste (es. Se o prelievo é stato eseguito troppo precocemente rispetto all'ipotetico momento di esposizione) ou se a campione é stato prelevato, trasportato ou conservato impropriamente.
Por isso, o produto do kit evidenciado que um resultado negativo do teste não exclui a possibilidade de infecção de SARS-CoV-2 e a negatividade do campo, uma fronteira de forte sospetto de COVID-19, dovrebbe essere confermata mediante teste molecolare.
Eu testo molecolari sembrano avere una maggiore sensibilità prima della comparsa dei sintomi, mentre nella fase iniziale imediatamente sucessiva all'inizio dell'infezione i teste rapidi antigenici e quelli molecolari hanno una sensibilità símile, rendendo utile l'uso anche dei primi (2).
Além disso, il test rapido antigenico può essere utilizzato per l'identificazione dei contatti asintomatici dei casi, anche se questo tipo di test non è specificamente autorizzato per questa destinazione d'uso, poiché è stato dimostrato che i casi asintomatici hanno cariche virali simili ai ai sintomatici (10).
Purtroppo, fino e oggi non we are enoughi studi publicati che, a fronte di contesti specifici and di una ampia casistica, forniscano indicazioni sulla sensibilità e specificità di questi test rapidi.
Allo stato attuale, i dati disponibili dei vari test for this parametri son quelli dichiarati do produttore: 70-86% per the sensibilità and 95-97% by the specificità (11-14)
La Foundation for Innovative New Diagnostics (FIND) (https://www.finddx.org/covid19/pipeline/?section=show-all#diag_tab) ha creato una piattaforma online em rapida evoluzione che raccoglie una vasta série de saggi por SARS -CoV-2 che vanno dalle prime fasi di sviluppo fino alla piena approvazione normativa.
Riguardo testou seu tampão salivar, se o dispositivo de recuperação é o mesmo, pode mudar o campo analizador para mudar as características de sensibilidade e especificidade do teste.
Em conclusão, a sensibilidade e a especificidade do teste antigenici rapidi dovranno essere valutate per i loro valori predittivi nel corso del loro sviluppo tecnologico.
È importante la condivisione dei dati a livello locale / regionale / nazionale delle validazioni su vari tipi di test antigenici rapidi, inclusive quelli salivari, in commercio nel nostro paese.
Teste sierologici
Eu testo sierologici rilevano l'esposizione al virus SARS-COV- 2 ma não foi grado di confermare or meno una infezione in atto.
Por questão, em caso de positivação, você precisa de um teste molecolare su tampone per conferma.
Come a circolare del Ministero della Salute 16106 del 9 de maio de 2020, si ribadisce che “la qualità e l'affidabilità di un test dipendono in particolare dalle due caratteristiche di specificità and sensibilità, e pertanto, sebbene non esse sussistano in relazione ad obblighi , è fortemente raccomandato l'utilizzo di test del tipo CLIA e / o ELISA che abbiano una specificità non inferiore al 95% e una sensibilità non inferiore al 90%, al fine di ridurre il numero di risultati false positivi and false negativi.
Al di sotto di queste soglie, l'affidabilità del risultato ottenuto non é adeguata alle finalità per cui i test vengono eseguiti ”.
O documento completo em matéria de teste por COVID-19 publicado pela FNOMCEO e riferimento por i medici italiani
Copia_DocPrincipal_COVID_19__test_v4k_lastTeste COVID-19, bibliografia
1. Organização Mundial da Saúde. Perfis de produtos de destino para diagnóstico de prioridade
tiques para apoiar a resposta à pandemia COVID-19 v.1.0. Genebra: OMS; 2020
2. Mina MJ, Parker R, Larremore DB. Repensando a sensibilidade do teste Covid-19 - Uma estratégia de contenção. N Engl J Med 2020, 30 de setembro. DOI: 10.1056 / NEJMp2025631
3. Comissão Europeia. Desempenho atual dos métodos e dispositivos de teste COVID-19 e critérios de desempenho propostos (16 de abril de 2020). Bruxelas: CE; 2020. https://ec.europa.eu/docsroom/documents/40805.
4. Comissão Europeia. Banco de dados de dispositivos de diagnóstico in vitro e métodos de teste COVID-19. Bruxelas: CE; 2020. https://covid-19-diagnostics.jrc.ec.europa.eu/ ).
5. Ministero della salute. Pandemia di COVID-19 - Aggiornamento delle indicazioni sui test diagnostici and sui criteri of adottare nella determinação delle priorità. Aggiornamento delle indicazioni relative alla diagnosi di laboratorio (0011715-03 / 04/2020). Roma: Ministero della Salute; 2020.
6. Mancini F, Barbanti F, Scaturro M, et al. Gerenciamento de laboratório para detecção de SARS-CoV-2: uma combinação amigável da abordagem de tratamento térmico e teste rt-Real-time PCR. Emerg Microb Infect. 2020; 9 (1): 1393- 1396. DOI: 10.1080 / 22221751.2020.1775500.
7. Fomsgaard AS, Rosenstierne MW. Um fluxo de trabalho alternativo para a detecção molecular de SARS CoV-2 - escapar da escassez de kits de extração de NA, Copenhagen. Dinamarca. Euro Surveill. 2020; 25: 2000398. doi: 10.2807 / 1560- 7917.ES.2020.25.14.2000398
8. Cheng MP, Papenburg J, Desjardins M, et al. Teste de diagnóstico para Coronavirus-2 relacionada à síndrome respiratória aguda grave: uma revisão narrativa [publicado online antes da impressão, em 2020 de abril de 13]. Ann Intern Med. 2020: M201301 10.7326 / M20-1301.
9. Centros para Controle e Prevenção de Doenças. Visão geral dos testes para SARS-CoV-2 (COVID-19). Atlanta, GA: CDC; 2020. https://www.cdc.gov/coronavirus/2019-ncov/hcp/testing-overview.html
10. Organização Mundial de Saúde. Detecção de antígeno no diagnóstico de infecção por SARS-CoV-2 usando imunoensaios rápidos. Orientação provisória. Genebra: OMS; 2020. https://www.who.int/publications/i/item/antigendetection-in-the-diagnosis-of-sars-cov-2infection-using-rapid-immunoassays
11. Dinnes J, Deeks JJ, Adriano A, Berhane S, Davenport C, Dittrich S, Emperador D, Takwoingi Y, Cunningham J, Beese S, Dretzke J, Ferrante di Ruffano L, Harris IM, Price MJ, Taylor-Phillips S , Hooft L, Leeflang MMG, Spijker R, Van den Bruel A. Rapid, antígeno de ponto de atendimento e testes de base molecular para o diagnóstico de infecção por SARS-CoV-2. Cochrane Database of Systematic Reviews 2020, Issue 8. Art. Nº: CD013705. DOI: 10.1002 / 14651858.CD013705
12. Castro R, Luz PM, Wakimoto MD, Veloso VG, Grinsztejn B, Perazzo H. COVID-19: uma meta-análise da precisão dos testes diagnósticos de ensaios comerciais registrados no Brasil [publicado online antes da impressão, 2020 de abril de 18]. Braz J Infect Dis. 2020; S14138670 (20): 530029. DOI: 10.1016 / j.bjid.2020.04.003
13. Russo A, Minichini C, Starace M, et al. Situação atual do diagnóstico laboratorial para COVID-19: uma revisão narrativa. Infect Drug Resist. 2020; 13: 2657-2665. doi: 10.2147 / IDR.S264020
14. Tubulação de diagnóstico SARS-CoV-2. https://www.finddx.org/covid-19/pipeline/ .
Para saber mais:
Il tampone salivare per i bambini inventato de 4 scienziate (e mamme) di UniMi



