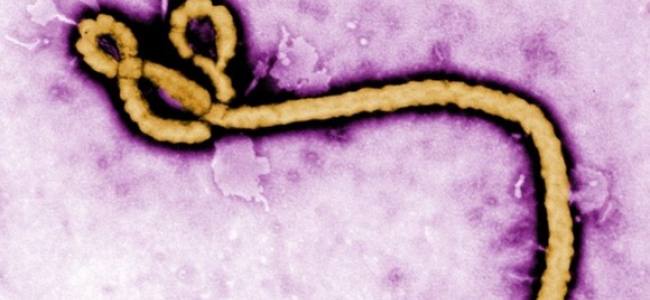
エボラについての事実、嘘と物語
イギリスの新聞The Guardianに関する最近の記事(The Guardian、月曜日22 12月、2014)は、シエラレオネのエボラとの戦いにおけるEmergencyの取り組みについて、根拠のない推測、嘘、および未確認の情報をいくつか報告しました。 これらの根拠のない非難のいくつかはまたBMJの記事(http://www.bmj.com/content/349/bmj.g7198/rapid-responses)への応答として同じグループのNHSの医者によって書かれていて報告されているAljazeera Webサイトの記事に。
「ラッカセンターの死亡率が約67%」というのは間違っています。 ラッカセンターは、9月の18から12月の10までの間、隔離と治療の両方の部門として機能してきました。 EVDと確定診断された2014患者の治療を受けたセンターの総合致死率(CFR)は122%で、57.4は生存者で死亡しています(これらの患者の52は非常に危険な状態にあり、その後70時間以内に死亡しました)。入場)。 WHOの専門家によっても述べられているように、他のエボラ治療センターからのCFRは常に利用可能ではなく、あまり信頼できません。 最近のWHO報告では、治療センターのCFRはおよそ13%であると推定しています(WHOシチュエーション報告、24 12月60)。
アミオダロンが人間でテストされていない薬であるというのは誤りです。 それは40年以来臨床心臓病学で使用され、危機的な状態や集中治療を必要とする患者でさえ、何百万もの人々に処方されています。 実際、アミオダロンのような安全性プロファイルがよく知られている薬はほとんどありません。これは、アスピリン、メトホルミンなどの長期使用によって確認されています。 アミオダロンがEVDの治療でまだテストされていないのは事実です(しかし、この使用の受容性については以下を参照してください)。 それにもかかわらず、臨床研究では、新しい目的のための既知の薬剤の「適応外」使用が広く認められています。 「エボラウイルス性疾患に対する未登録の介入の使用に関する倫理的考慮事項」で、WHOパネルは、実験室および動物モデルで有望な結果を示したが、安全性と有効性についてまだ評価されていない証明されていない介入を提供することは倫理的に許容できると述べました。潜在的な治療または予防として人間に。 この原則がアミオダロンのような安全な薬に適用されるべきではない理由はわかりません。
緊急事態が「注意深く管理された条件」の外で「無謀な」方法でアミオダロンを使用したと述べることは誤りで非常に不快です。 それどころか、アミオダロンは集中治療室の患者のモニタリングで使用されてきました:非侵襲的動脈圧、ECG(QT間隔の決定を含む)、心拍数、酸素飽和度、電解質。
DFIDからの要請に応じて、緊急事態が中止されてアミオダロンが投与されていたのは間違いです。 DFIDは、技術的な評価や患者の治療法や臨床的処置の決定には関与していない。
緊急事態は当初からエボラの文脈で科学的知識を促進するために適切な無作為化臨床試験をデザインする必要があると認めた。 EASE(エボラに対する緊急アミオダロン研究)と名付けられた研究はClinicaTrials.govに登録されており、すでにイタリアのレッジョ・エミリアのIRCCSの倫理委員会およびイタリアの国立感染症研究所の倫理委員会によって承認されていますL。 Spallanzani、ローマ。 緊急事態は、EASE試験がシエラレオネの倫理科学委員会に提出されたときに、「ケースバイケース」でのアミオダロンの使用を中止することを決定しました。
DFIDがNHSスタッフを緊急施設から撤退させたのは誤りです。 緊急事態は、チームのすべてのメンバーとその臨床的アプローチについて話し合う際に、常に非常にオープンで透明性があります。 NHSチームとのXNUMX週間以上の繰り返しの話し合いの後、緊急事態は、組織との協力をやめることができると不安を感じている人々に同意しました。 DFIDによって承認されたアプローチも。 それどころか、私たちと一緒に働き続けたいと思っていたNHSチームの一部は、最終的にすべてのチームが去るまで、プレッシャーにさらされ、同僚から脅迫されました。 それにもかかわらず、同じチームの一部のメンバーは、将来、緊急事態で再び仕事をするために戻ってくる意思をすでに表明しています。
私たちの研究はこれまでDFIDとNHSの両方で共有されていたUK Medによって行われた品質評価調査によって非常に肯定的に評価されていたので、緊急事態はこの行動に非常に驚いています。 さらに、Emergencyの臨床診療は、Sierra Leoneの最高医療責任者によって正式に承認されており、組織は、新たに発行されたWHO Sierra Leone適応VHFポケットガイドの開発において重要な情報を提供しました。
「救急スタッフの主な焦点は、患者が十分に水分補給され、清潔で快適であることを保証するのではなく、患者がこれらの薬を確実に受け取れるようにすることでした」というのは誤りです。 WHOおよび緊急臨床ガイドラインに記載されているように、患者の水分補給は、支持療法の最も重要な要素の350つです。 患者は、量と電解質のバランスを回復するために、122日あたり数リットルの点滴で積極的に水分補給されています。 Lakkaの名簿は、最適な患者の出席を保証するために編成されました。患者XNUMX人あたりXNUMX日約XNUMX分の医療処置により、正確な監視が可能な限り最高の標準治療を提供し、高水準の衛生状態を確保します。 NHSチームが、自宅にいて批判を行うのではなく、病院で患者の世話をすることに時間を費やしていたとしたら、彼らは私たちの患者管理についてはるかに明確な状況を把握していたでしょう。 Lakkaで治療されたXNUMX人のエボラ確認患者のうち、実際に観察された患者はごくわずかであり、非常に限られた期間でした。 EMERGENCYは、一部のNHSスタッフの行動とUK-Medによるチームの管理に関する公式の苦情報告をDFIDと正式に共有しました。
緊急事態が患者の同意を求めないことを述べるのは虚偽で中傷的です。 20年以来、世界中のすべてのEmergencyの施設で、患者、または適切な場合には親類は、いかなる医学的または外科的処置についてもインフォームドコンセントを提供するよう求められています。
それどころか、「西洋の患者」と比較して、アフリカの患者に彼らの「同意」を非常に異なる方法で(「第二種の方法」と言うことができる)求めることを求めている人はいないでしょう。
何とか薬を乱す
国際的な専門家や科学者との徹底的な議論の結果、EmergencyはSierra LeoneのEbola Virus Disease(EVD)に罹患した一部の患者にamiodaroneと呼ばれる薬を投与することを決めました。 この薬物は「規格外」で、つまり通常の治療適応外に使用されてきました。
緊急事態は、この決定は科学的かつ倫理的に適切であると考えている。なぜなら、インビトロで実施される多くの試験が、アミオダロンがエボラウイルスに対する特異的な抗ウイルス作用を有することを証明したからである。 (J Antimicrob Chemother。2014 Aug; 69(8):2123-31。doi:10.1093 / jac / dku091。Epub 2014 Apr 7)を、臨床心臓病学において一般的に処方される用量で投与する。
それを受け取ったすべての患者は(臨床プロトコルまたは試験の外で、医学的な「ケースバイケース」の決定に基づいて)、治療を通して非常に注意深く監視されています。
死亡率が非常に高い病気に直面しており、治療法が特定されていない疾患に遭遇した場合、エボラに対して潜在的に有益な影響を及ぼす薬剤の使用は、薬が安全で副作用があれば、知られている。
ラコカでアミオダロンを使用するかどうかの決定は、シエラレオネの保健当局と共有され、22nd 9月2014と厚生労働省に署名した覚書の承認を受けた。
残念なことに、amiodaroneには大きな問題があり、「Ebolaとの戦い」でさまざまな方法で関わる「専門家」の多くには耐えられません。amiodaroneは、だれにも利益をもたらしません。 それは、長年の特許から、ジェネリック医薬品であるという利益を生み出すことができず、1タブレットあたり数セントという非常に低いコストで簡単に製造できるということです。
明らかに、緊急事態はアミオダロンがエボラに対して働いていると述べていません。 そう言うと、私たちが提案したように、ランダム化臨床試験でテストする必要があります。 それにもかかわらず、ヨーロッパまたは米国でのみ非常に限られた量で非常に高いコスト(数百)で入手可能な新薬(実際には「テストされていない」)にのみ焦点を当てながら、アミオダロンのテストの承認を拒否することは科学的な観点から愚かであると信じています各用量の数千米ドル)。 これは、エボラ出血熱の敗北に貢献する機会を失う可能性があります。
Lakkaでの私たちの経験
緊急時に管理されるLakka Ebola Treatment Unitでアミオダロンを投与された患者の観察データは以下のように要約できます:
48患者は、10 mg / kg / dieを超えずに有意な抗ウイルス作用を発現させるために、20までの血清血漿濃度を得ることを目的とする用量で薬剤を投与した。
アミオダロンは最初の3日にIV投与され、次の7日に経口投与された。
amiodarone(非常に重篤な状態で24が出現し、入院から6時間以内に死亡した患者)の24死亡を記録しました。 このグループ内の死亡率は50%でした。 (これらの42,8早期死亡を除外した場合は6%、18患者では42死亡)。
以前に述べたように、ラクカセンターの全体的なCFRは、57.4%、122患者、52.3%であった。
薬物安全性に関しては、2患者のみで軽度の副作用が観察されている.1つは収縮期圧が20%低下し、もう1つは徐脈を登録した(心拍数60拍/分)。 両方の患者が無症状のままであったにもかかわらず、私たちの臨床医はアミオダロンの投与を中止することに決めました。
これらの予備的観察は、私たちの意見では、アミオダロンは患者にとって「有害」ではなく、有益でさえあるかもしれないと述べる確かな倫理的および科学的根拠を提供し、臨床試験の理論的根拠を強化します。



