X連鎖劣性遺伝:分子メカニズムを特定するための新しい研究
Acrogigantism:Humanitasの研究者であるGiampaolo Trivellin博士の研究プロジェクトは、2020年2018月に開始され、MarieSkłodowskaCurieAction-IndividualFellowship 2021の受賞とTelethonFoundationの助成金(XNUMX年XNUMX月に開始)のおかげで実施されました。最初の重要な結論
101年23月2022日に科学雑誌TheAmerican Journal of Human Geneticsに掲載された研究「重複はクロマチン構造を破壊し、GPRXNUMX-エンハンサーコミュニケーションをX連鎖遺伝学で再配線する」に示されているように、トリベリン博士は病理学的メカニズムへの洞察を得ることができました根底にあるX連鎖性アクロギャンティズム(X-LAG)。
X-LAGはまれな遺伝性疾患であり、現在世界中で約40人が診断されています。つまり、下垂体の機能不全に関連する病状である下垂体巨人症の患者の10%です。
Acrogigantism:それは何ですか
X連鎖性のアクロギガンティズムは、2014年にTrivellin博士のチームによって最初に説明され、X染色体にある遺伝的欠陥によって引き起こされる状態です。具体的には、GPR101と呼ばれる膜受容体の生成に関する指示を含む遺伝子の重複です。
GPR101の重複は、成長ホルモン(GH)の過剰分泌を引き起こす下垂体の腫瘍に関連しています。
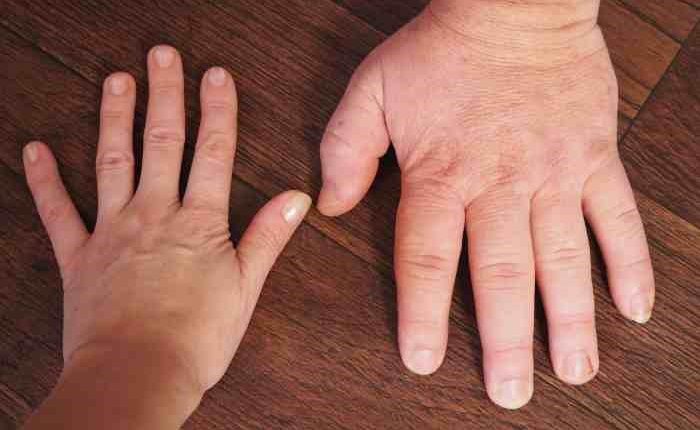
アクロギガンティズムのさまざまな臨床症状の中で、最も明白なのは患者の過度の体の成長であり、治療せずに放置すると、通常、身長が2メートルを超えます。
X-LAGの治療法はありませんが、現在、外科手術、内科療法、そしてまれに放射線療法を含む学際的なアプローチで治療することができます。
Acrogigantism Research Study
Trivellin博士と彼の研究チームは、GPR101遺伝子の役割と、これまで知られていなかった下垂体腫瘍での顕著な発現を引き起こす分子メカニズムを調査しました。
この研究は、その過剰発現の原因が、遺伝子が存在するクロマチンドメインの変化にあることを示しました。
この変化は、病気に関連する重複によって引き起こされます。
私たちのDNAは、クロマチンドメイン、つまりTAD(トポロジー関連ドメイン)に分割されます。これらのドメインは、その中にある遺伝子を残りのゲノムから分離するように機能します。
この区画化により、遺伝子発現を促進する調節要素(エンハンサー)の作用が、同じクロマチンドメイン内にある遺伝子にのみ限定されることが保証されます。
X-LAG患者でGPR101と一緒に通常複製される他の遺伝子とは異なり、GPR101は、他の遺伝子から分離された、それ自体のクロマチンドメイン内の唯一の遺伝子です。
患者では、遺伝子重複によって引き起こされるクロマチンドメインの再配列があり、GPR101遺伝子が他の遺伝子のエンハンサー配列から分離されなくなったが、現在はそれらと相互作用する新しいクロマチンドメインをもたらします。
患者の腫瘍におけるGPR101の顕著な発現につながるのは、これらの新しい病理学的相互作用です。
アクロギガンティズム、将来の展望
Trivellin博士の研究によって内分泌学で初めて説明されたこのメカニズムの発見は、下垂体の疾患と同様の病理学的メカニズムを通じて発症する可能性のある他の内分泌障害の両方について、さらなる研究の展望を開きます。
成長ホルモンの過剰産生につながる細胞内シグナルのカスケードのプロモーターであるGPR101受容体の過剰発現を決定するものを知ることは、巨人症に冒された患者の新しい治療の視点において基本となるでしょう。
これは、アクロギガンティズムの患者のGPR101と相互作用するエンハンサー配列を特異的に阻害する治療法の将来の開発に向けた最初のステップです。GPR101遺伝子の過剰発現をオフにすると、成長ホルモンの過剰分泌とそれに関連する衰弱症状が軽減されます。
また、
ダウン症の人のCOVID-19:死亡率は最大10倍高い。 ISSの研究



