Syndrome da distress respiratorio (ARDS): terapi, ventilazione meccanica, monitoraggio
La sindrome da distress respiratorio (på engelsk "acute respiratory distress syndrome" da cui l'acronimo "ARDS") è una patologia respiratoria determinata da varie årsak e caratterizzata da danno diffuso ai capillari alveolari che determina grave insufficienza alla respiratoria art constratmia di ossigeno
La ARDS è quindi caratterizzata da una diminuzione della concentrazione di ossigeno nel sangue, la quale è resistente alle O2 terapia, cioè tale concentrazione non sale in seguito alla somministrazione di ossigeno al paziente.
L'insufficienza respiratoria ipossiemica è dovuta ad una lesione della membrana alveolo-capillare, che aumenta la permeabilità vascolare polmonare, determinando un edema interstiziale ed alveolare.
BARELLE, VENTILATORI POLMONARI, SEDIE DA EVACUAZIONE: JEG PRODOTTI SPENCER NEL DOPPIO STÅR I NØDEXPO
Il trattamento dell'ARDS è, fondamentalmente, di supporto e består av:
- trattamento della causa a monte che ha scatenato l'ARDS;
- mantenimento di una adeguata ossigenazione tissutale (ventilasjon ed assistenza cardiopolmonare);
- supporto nutrizionale.
La ARDS è una sindrome scatenata da molti e differenti fattori precipitanti che determinano un danno polmonare simile
Su alcune delle cause di ARDS non è possibile intervenire, ma, nei casi in cui ciò sia fattibile (come nel caso dello shock o delle sepsi), un trattamento precoce ed efficace diventa cruciale per limitare la gravità della sindrome e per aumentare sopravvivenza del paziente.
Il trattamento farmacologico della ARDS è diretto a correggere i disturbi di base ed a fornire un sostegno alla funzione cardiocircolatoria (ad esempio, antibiotici per il trattamento dell'infezione e vasopressori per il trattamento dell'ipotensione).
L'ossigenazione tissutale dipende da un adeguato rilascio di ossigeno (O2del) che è funzione dei livelli arteriosi di ossigeno e della gittata cardiaca.
Ciò implica che, sia la ventilazione che la funzione cardiaca, sono cruciali per la sopravvivenza del paziente.
La ventilazione meccanica a pressione teleespiratoria positiva (PEEP) è essenziale per garantire una adeguata ossigenazione arteriosa nei pazienti con ARDS.
La ventilazione a pressione positiva, comunque, può, contestualmente al miglioramento dell'ossigenazione, ridurre la gittata cardiaca (vedi oltre). Il miglioramento dell'ossigenazione arteriosa è di scarsa o nulla utilità se il contemporaneo aumento della pressione intratoracica induce una corrispondente riduzione della gittata cardiaca.
Di conseguenza, il livello massimo di PEEP tollerato dal paziente è in genere dipendente dalla funzione cardiaca.
Una grave ARDS può determinare il decesso per ipossia tissutale, quando una terapia massimale con liquidi ed agenti vasopressori non migliorino adeguatamente la gittata cardiaca, per quel dato liveello di PEEP necessario a garantire un efficiente scambio gassosomon pol.
Nei pazienti più gravi, ed in particolare in quelli sottoposti a ventilazione meccanica, si determina spesso uno stato di malnutrizione.
Gli effetti della malnutrizione a livello polmonare comprendono: immunosuppressione (ridotta attività macrofagica e dei linfociti T), attenuato stimolo respiratorio da parte dell'ipossia e della ipercapnia, alterata funzione del surfattante, ridotta massama dei muscoli intercolione dei muscoli respiratori, i relazione all'attività catabolica dell'organismo, pertanto la malnutrizione può influenzare molti fattori critici, non solo per l'efficacia della terapia di mantenimento e di supporto, ma anche per lo svezzamento dal ventilatore meccan.
Se praticabile, è preferibile far ricorso ad un'alimentazione di tipo enterale (somministrazione di cibo mediante un sondino nasogastrico); ma se la funzione intestinale è compromessa, diventa necessaria la via parenterale (endovenosa), per infondere tilstrekkelig quantità di proteiner, grassi, carboidrati, vitamin e minerali al paziente.
Ventilazione meccanica nella ARDS
La ventilazione meccanica e la PEEP non prevengono né trattano direttamente la ARDS ma, piuttosto, mantengono in vita il paziente fino alla risoluzione della patologia di base ed alla ripresa di una adeguata funzione polmonare.
Il pilastro della ventilazione meccanica continua (CMV) i corso di ARDS består av nella convenzionale ventilazione "volum-dipendente", med impiego di volumi tidal di 10-15 ml/kg.
Nelle fasi akutt della malattia, oftere enn un'assistenza respiratoria total (i genere mediante ventilazione "assistenza-controllo" eller ventilazione intermittente obbligata [IMV]).
Un'assistenza respiratoria parziale viene in genere praticata i fase di guarigione eller di svezzamento dal ventilatore.
La PEEP può determinare la ripresa della ventilazione a livello di zone atelettasiche, trasformando aree polmonari precedentemente sede di shunt in unità respiratorie funzionali, conseguente miglioramento della ossigenazione arteriosa ad una più bassa frazione di ossO2 inspirato.
La ventilazione di alveoli già atelettasici aumenta, inoltre, la capacità funzionale residua (FRC) og la compliance polmonare.
Generalmente, l'obiettivo della CMV con PEEP è quelo di raggiungere una PaO2 maggiore di 60 mmHg ad una FiO2 inferior a 0.60.
Anche se la PEEP è viktig per il mantenimento di uno scambio polmonare gassoso adeguato nei pazienti con ARDS, sono possibili effetti collaterali.
Possono verificarsi una riduzione della compliance polmonare per sovradistensione alveolare, una riduzione del ritorno venoso e della gittata cardiaca, un aumento della PVR, un aumento del postcarico del ventricolo destro, o un barotrauma.
Per questi motivi, foreslår du å bruke livelli av PEEP "ottimali".
Il livello di PEEP ottimale viene in genere definito come il valore al quale si ottiene il miglior O2del ad una FiO2 inferiore a 0,60.
Valori di PEEP i grado di migliorare l'ossigenazione, ma che riducano significativamente la gittata cardiaca non sono ottimali, perché in questo caso risulta ridotto anche l'O2del.
La pressione parziale di ossigeno a livello del sangue venoso misto (PvO2) fornisce informazioni sull'ossigenazione tissutale.
En PvO2 lavere enn 35 mmHg è indikativ for en ossigenazione tissutale non ottimale.
Una riduzione della gittata cardiaca (che si può verificare in corso di PEEP) determina una bassa PvO2.
Per questa ragione, la PvO2 può essere utilizzata anche per la determinazione della PEEP ottimale.
L'insuccesso della PEEP med CMV convenzionale rappresenta il più frequente motivo per cui si renda necessario passere ad una ventilazione con rapporto inspiratorio/espiratorio (LE) inverso o ad alta frequenza.
La ventilazione con rapporto I:E inverso viene, attualmente, praticata più spesso di quella ad alta frequenta.
Essa fornisce risultati migliori con il paziente paralizzato ed il ventilatore temporizzato in modo che ogni nuovo atto respiratorio inizi non appena l'espirazione precedente abbia raggiunto il livello ottimale di PEEP.
La frequenza respiratoria può essere ridotta prolungando l'apnea inspiratoria.
Ciò determina spesso una riduzione della pressione intratoracica media, malgrado l'aumento della PEEP, ed induce, quindi, un miglioramento del O2del mediato dall'aumento della gittata cardiaca.
Ventilazione a pressione positiva ad alta frequenta (HFPPV), oscillazione ad alta frequenta (HFO), e ventilazione a "jet" ad alta frequenta (HFJV) sono methodiche in grado, a volte, di migliorare la ventilazione e l'ossigenazione senza far ricors ad elevati volumi o pressioni polmonari.
Solo la HFJV è stata diffusamente applicata nel trattamento dell'ARDS, senza che ne siano stati dimostrati in waya conclusiva significativi vantaggi rispetto alla CMV convenzionale con PEEP.
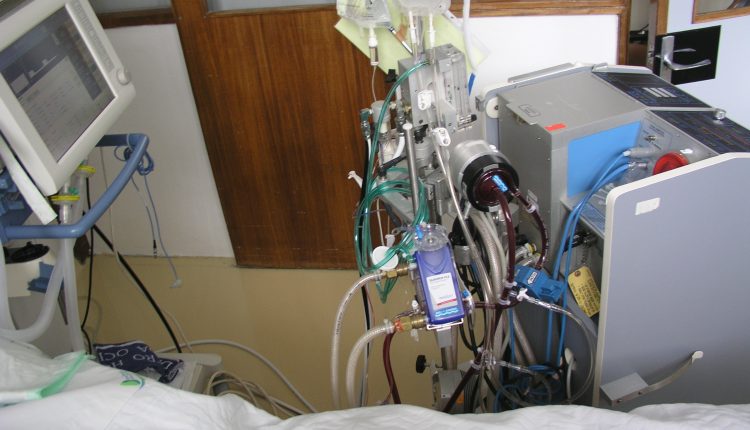
L'ossigenazione extracorporea su membrana (ECMO) venne studiata, negli anni '70, come metodica in grado di garantire un'adeguata ossigenazione senza far ricorso ad alcuna forma di ventilazione meccanica, lasciando il polmone libero di guarire seniliza de sottopla responsS allo stress rappresentato dalla ventilazione a pressione positivea.
Sfortunatamente, i pazienti tanto gravi da non rispondere adeguatamente alla ventilazione convenzionale ed essere quindi eligibili per la ECMO, presentavano lesioni polmonari così alvorlige che andarono comunque incontro a fibrosi polmonunaareon normal e pi non recupareo pi non recuperareo.
Svezzamento dalla ventilazione meccanica nell'ARDS
Prima di staccare il paziente dal ventilatore, è necessario assicurarsi delle sue possibilità di sopravvivere senza assistenza respiratoria.
Gli indici meccanici, come pressione inspiratoria massima (MIP), capacità vitale (VC), e volum tidal spontaneo (VT) valutano la capacità del paziente di trasportare aria dentro e fuori il torace.
Nessuna di queste misure, comunque, fornisce informazioni sulla resistenza al lavoro da parte dei muscoli respiratori.
Alcuni indici fisiologici, kommer il pH, il rapporto spazio morto/volum tidal, la P(Aa)O2, lo stato nutrizionale, la stabilità cardiovascolare, e l'equilibrio metabolico acido-base riflettono le condizioni generali del paziente e la sua capacità di tollerare lo stress dello svezzamento dal ventilatore.
Lo svezzamento dalla ventilazione meccanica avviene progressivamente, in modo da assicurarsi che le condizioni del paziente siano enoughi a garantire una respirazione spontanea, prima di rimuovere la cannula endotracheale.
Questa fase inizia in genere quando il paziente è, dal punto di vista medico, stabil, con una FiO2 inferiore a 0,40, una PEEP uguale o inferiore a 5 cm H2O ed i parametri respiratori, cui si è fatto riferimento in pre- , indichino una ragionevole possibilità di ripresa della ventilazione spontanea.
La IMV è una popolare metodica per lo svezzamento dei pazienti con ARDS, perché consente l'uso di una modesta PEEP fino al momento della estubazione, facendo in modo che il paziente affronti gradualmente lo sforzo richiesto dalla respirazione spontanea.
Durante questa fase di svezzamento, è viktig un attento monitoraggio per garantirne il successo.
Modifikasjoner della pressione arteriosa, aumento della frequenza cardiaca eller respiratoria, riduzione della saturazione arteriosa di ossigeno misurata con ossimetria di polso, e peggioramento delle funzioni mentali, sono tutti elementi che indicano l'insuccesso della procedura.
Un graduale rallentamento dello svezzamento può bidra til en prevenire un insuccesso legato ad esaurimento muscolare, che si può verificare nel corso della ripresa della respirazione autonoma.
Monitoraggio in corso di ARDS
Il monitoraggio arterioso polmonare consente di misurare la gittata cardiaca e di calcolare l'O2del e la PvO2.
Questi parametri sono essenziali per il trattamento di eventuali complicanze emodinamiche.
Il monitoraggio arterioso polmonare consente anche di misurare le pressioni di riempimento del ventricolo destro (CVP) e del sinistro (PCWP), parametri utili per determinare la gittata cardiaca ottimale.
Un cateterismo arterioso polmonare per il monitoraggio emodinamico diventa importante nel caso la pressione arteriosa si riduca tanto da richiedere un trattamento con farmaci vasoattivi (come dopamina, norepinefrina) o qualora la funzione polmonare si deteriori fino a cm10 renderi ne EP 2 cm renderi.
Anche il riscontro di una instabilità pressoria, tale da richiedere ingenti infusioni di liquidi, in un paziente già in precarie condizioni cardiache o respiratorie, può richiedere il posizionamento di un catetere in arteria polmonare ed il monitoraggio emodcessnamico si renminia primaria farm vasoativi.
Ventilasjonen er positiv og endres i data del monitoraggio emodinamic, bestemmer un aumento fittizio dei valori della PCWP.
Elevati valori di PEEP possono trasmettersi al catetere di monitoraggio ed essere responsabili dì un aumento dei valori calcolati di CVP e PCWP non corrispondente al reale (43).
Questa evenienza è più probabile se la punta del catetere si trova in prossimità della parete anteriore del torace (zona I), con il paziente supino.
La zona I è l'area polmonare non declive, dove i vasi sanguigni sono minimamente distesi.
Se l'estremità del catetere si localizza a livello di uno di essi, i valori della PCWP saranno notevolmente influenzati dalle pressioni alveolari, e risulteranno, pertanto, unaccurati.
La zona III corrisponde all'area polmonare più declive, dove i vasi sanguigni sono quasi semper distesi.
Se l'estremità del catetere si localizza i quest'area, le misurazioni effettuate saranno influenzate solo molto marginalmente dalle pressioni di ventilazione.
Il posiziona mento del catetere a liveello della zona III può essere verificato effettuando una radiografia del torace in proiezione laterale, che ne evidenzierà la punta al di sotto dell'atrio sinistro .
Med statisk samsvar (Cst) fornisce utili informazioni sulla rigidità del polmone e della parete toracica, mentre la compliance dinamica (Cdyn) valuta le resistenze delle vie aeree.
La Cst si calcola dividendo il volum tidal (VT) per la pressione statica (al plateau) (Pstat) meno la PEEP (Cst = VT/Pstat – PEEP).
La Pstat si calcola durante una breve apnea inspiratoria dopo un respiro massimale.
I praksis, ciò può essere ottenuto utilizzando il comando pausa del ventilatore meccanico eller mediante occlusione manuale della linea espiratoria del circuito.
La pressione si controlla sul manometro del ventilatore durante l'apnea eve essere inferiore all pressione massima delle vie aeree (Ppk).
La compliance dinamica si calcola in maniera analoga, anche se, in questo caso si fa riferimento all Ppk, invece che alla pressione statica (Cdyn = VT/Ppk – PEEP).
La Cst normale è compresa tra 60 e 100 ml/cm H2O e può ridursi sino a circa 15 o 20 ml/cm H20 nei casi gravi di polmonite, ødem polmonare, atelettasia, fibrosi ed ARDS
Poiché, per superare le resistenze delle vie aeree durante la ventilazione, è necessaria una certa pressione, una parte della pressione massima sviluppata durante la respirazione meccanica, rappresenta la resistenza al flusso incontrata a liveello dellle delle delle vie circuit.
Pertanto, la Cdyn misura la compromissione globale dei flusso a livello delle vie aeree, dovuta a modificazioni sia della compliance che delle resistenze.
La Cdyn normale è compresa tra 35 e 55 ml/cm H2O, ma può essere negativamente influenzata dalle stesse patologie che riducono la Cstat, ed inoltre dai fattori in grado di modificare le resistenze (broncocostrizione, edema delle vieenzonieaeree, dicrezionieecompression, delle vie aeree ad opera di una neoplasia).
Å utdype:
Emergency Live ancora più…live: Last ned ny app gratis for iOS og Android
Ansiolitici e sedativi: ruolo, funzione e gestione con intubazione og ventilazione meccanica
Va e vieni: quando si usa? Hvor forskjellig rispetto al comune AMBU?
Soccorso vitale al traumatizzato: ecco quali-prosedyre vanno adottate
Pallone Ambu: caratteristiche e come si usa il pallone autoespandibile
AMBU: l'incidenza della ventilazione meccanica sull'efficacia della RCP
Kom og ventilasjon som ikke er invasiv og positiv
Ventilazione meccanica o artificiale: i differenti tipi e le indicazioni nell'utilizzo
Intubazione: rischi, anestesi, rianimazione, dolore alla gola
Gestione delle vie aeree dopo un incidente stradale: uno sguardo d'insieme
Distress respiratorio: kvali sono i segni di sofferenza respiratoria nei neonati?



