Akrogigantyzm sprzężony z chromosomem X: nowe badanie mające na celu identyfikację mechanizmów molekularnych
Akrogigantyzm: projekt badawczy dr Giampaolo Trivellina, badacza Humanitas, rozpoczęty w marcu 2020 r. i realizowany dzięki wygraniu Marie Skłodowska Curie Action-Individual Fellowship 2018 oraz grantu Fundacji Telethon (rozpoczęty w czerwcu 2021 r.), osiągnął szczyt pierwszy ważny wniosek
Jak określono w badaniu „Duplikacje zaburzają architekturę chromatyny i przekierowują komunikację wzmacniacza GPR101 w akrogantyzmie sprzężonym z chromosomem X”, opublikowanym 23 lutego 2022 r. w czasopiśmie naukowym The American Journal of Human Genetics, dr Trivellin był w stanie uzyskać wgląd w mechanizmy patologiczne leżący u podstaw akrogyantyzmu sprzężonego z chromosomem X (X-LAG).
X-LAG to rzadka choroba genetyczna, którą obecnie rozpoznaje się u około 40 osób na całym świecie, tj. 10% pacjentów z gigantyzmem przysadki, patologią związaną z dysfunkcją przysadki.
Arogigantyzm: co to jest
Akrogigantyzm sprzężony z chromosomem X został po raz pierwszy opisany przez zespół dr Trivellina w 2014 roku i jest stanem spowodowanym defektem genetycznym zlokalizowanym na chromosomie X, a dokładniej, duplikacją genu zawierającego instrukcje wytwarzania receptora błonowego o nazwie GPR101.
Duplikacja GPR101 jest związana z guzem przysadki mózgowej, który powoduje nadmierne wydzielanie hormonu wzrostu (GH).
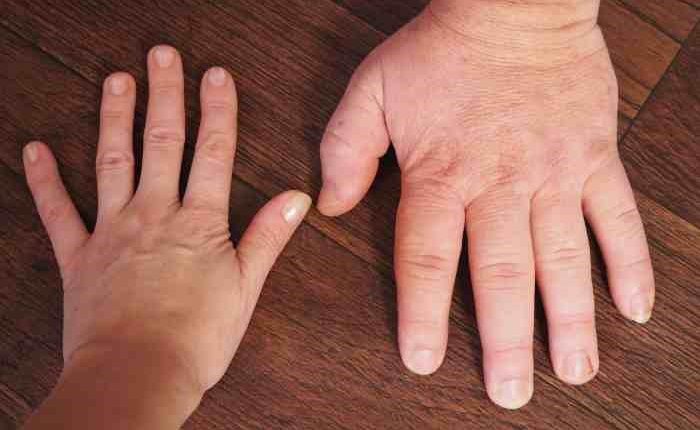
Wśród różnych klinicznych objawów akrogantyzmu najbardziej oczywistym jest nadmierny wzrost ciała pacjentów, którzy nieleczeni, zwykle przekraczają 2 metry wzrostu.
Chociaż nie ma lekarstwa na X-LAG, można ją obecnie leczyć za pomocą wielodyscyplinarnego podejścia, obejmującego operację, terapię medyczną i, rzadziej, radioterapię.
Badanie Akrogantyzmu
Dr Trivellin i jego zespół badawczy zbadali rolę genu GPR101 i mechanizmy molekularne, które powodują jego wyraźną ekspresję w guzach przysadki, mechanizmy, które do tej pory były nieznane.
Badanie wykazało, że przyczyną jego nadekspresji jest zmiana domeny chromatyny, w której znajduje się gen.
Ta zmiana jest indukowana przez duplikację związaną z chorobą.
Nasze DNA jest podzielone na domeny chromatyny lub TAD (domeny powiązane z topologią), których zadaniem jest izolowanie znajdujących się w nich genów od reszty genomu.
Ta kompartmentalizacja zapewnia, że działanie elementów regulatorowych (wzmacniaczy), które zwiększają ekspresję genów, ogranicza się tylko do genów znajdujących się w tej samej domenie chromatyny.
W przeciwieństwie do innych genów zwykle duplikowanych razem z GPR101 u pacjentów z X-LAG, GPR101 jest jedynym w własnej domenie chromatyny, izolowanym od innych.
U pacjentów dochodzi do rearanżacji domen chromatyny spowodowanej duplikacją genu, co skutkuje powstaniem nowej domeny chromatyny, w której gen GPR101 nie jest już oddzielony od sekwencji wzmacniających innych genów, ale teraz wchodzi z nimi w interakcje.
To właśnie te nowe patologiczne interakcje prowadzą do wyraźnej ekspresji GPR101 w guzach pacjentów.
Arogigantyzm, perspektywy na przyszłość
Odkrycie tego mechanizmu, opisanego po raz pierwszy w endokrynologii przez badania dr Trivellina, otwiera dalsze perspektywy badawcze zarówno nad chorobami przysadki mózgowej, jak i innymi zaburzeniami endokrynologicznymi, które mogą rozwijać się poprzez podobne mechanizmy patologiczne.
Wiedza o tym, co determinuje nadekspresję receptora GPR101, promotora kaskady sygnałów wewnątrzkomórkowych prowadzących do nadprodukcji hormonu wzrostu, będzie miała fundamentalne znaczenie w nowej perspektywie terapeutycznej dla pacjentów dotkniętych gigantyzmem.
Jest to pierwszy krok w kierunku przyszłego opracowania terapii, które specyficznie hamują sekwencje wzmacniające, które oddziałują z GPR101 u pacjentów z akrogigantyzmem: wyłączenie nadekspresji genu GPR101 zmniejszy nadmierne wydzielanie hormonu wzrostu i związane z tym wyniszczające objawy.
Czytaj także:
COVID-19 u osób z zespołem Downa: śmiertelność do 10 razy wyższa. Studium ISS
Zespół Downa i COVID-19, badania na Uniwersytecie Yale
Dzieci z zespołem Downa: oznaki wczesnego rozwoju choroby Alzheimera we krwi



