Неотложная педиатрия / Неонатальный респираторный дистресс-синдром (NRDS): причины, факторы риска, патофизиология
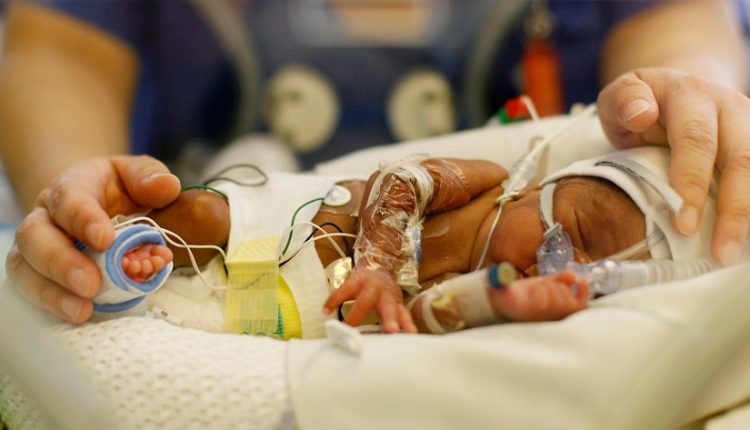
Респираторный дистресс-синдром новорожденных (NRDS) — респираторный синдром, характеризующийся наличием прогрессирующего ателектаза легких и дыхательной недостаточности, который в основном диагностируется у недоношенных новорожденных, еще не достигших полного созревания легких и адекватной продукции сурфактанта.
Синонимы детского респираторного дистресс-синдрома:
- ОРДС у младенцев (ОРДС означает острый респираторный дистресс синдром);
- ОРДС новорожденного;
- неонатальный ОРДС;
- педиатрический ОРДС;
- неонатальный РДС (РДС означает «респираторный дистресс-синдром»);
- респираторный дистресс-синдром новорожденных;
- острый респираторный дистресс-синдром ребенка;
- острый респираторный дистресс-синдром новорожденных.
Респираторный дистресс-синдром ранее был известен как «болезнь гиалиновых мембран», отсюда и аббревиатура «MMI» (сейчас вышла из употребления).
Респираторный дистресс-синдром младенцев по-английски называется:
- инфантильный респираторный дистресс-синдром (ИРДС);
- респираторный дистресс-синдром новорожденных;
- неонатальный респираторный дистресс-синдром (NRDS);
- синдром дефицита сурфактанта (SDD).
Синдром ранее был известен как «болезнь гиалиновых мембран», отсюда и аббревиатура «HMD».
Эпидемиология респираторного дистресс-синдрома новорожденных
Распространенность синдрома составляет 1-5/10,000.
Синдром поражает примерно 1% новорожденных.
Заболеваемость снижается с увеличением гестационного возраста, примерно с 50% у детей, родившихся в возрасте 26–28 недель, до примерно 25% в возрасте 30–31 недели.
Синдром чаще встречается у мужчин, представителей европеоидной расы, младенцев от матерей с диабетом и вторых недоношенных близнецов.
Хотя существует много форм дыхательной недостаточности, поражающих новорожденных, NRDS является преобладающей причиной у недоношенных.
Достижения в области предотвращения преждевременных родов и лечения неонатального NRDS привели к значительному снижению числа смертей от этого состояния, хотя NRDS продолжает оставаться важной причиной заболеваемости и смертности.
Подсчитано, что около 50 процентов смертей новорожденных имеют NRSD.
Из-за высокой смертности все врачи интенсивной терапии новорожденных должны уметь диагностировать и лечить эту распространенную причину дыхательной недостаточности.
Возраст начала
Возраст начала — неонатальный: симптомы и признаки респираторного дистресс-синдрома появляются у новорожденных вскоре после рождения или через несколько минут/часов после рождения.
ЗДОРОВЬЕ РЕБЕНКА: УЗНАЙТЕ БОЛЬШЕ О MEDICHILD, посетив стенд на EMERGENCY EXPO
Причины: дефицит сурфактанта
Младенец с РДС страдает дефицитом сурфактанта.
Сурфактант (или «легочный сурфактант») представляет собой липопротеиновое вещество, продуцируемое пневмоцитами типа II на альвеолярном уровне примерно с тридцати пятой недели гестационного возраста, и его основная функция заключается в снижении поверхностного натяжения путем обеспечения расширения альвеол во время дыхательных актов: его отсутствие поэтому сопровождается снижением альвеолярного расширения и тенденцией к закрытию с нарушенным газообменом, с нарушением нормального дыхания.
При рождении сурфактант должен вырабатываться в достаточном количестве и такого качества, чтобы предотвратить коллапс альвеол в конце выдоха.
Ответственными за выработку этого сурфактантно-активного вещества, столь важного для постнатальной функции легких, являются функционально интактные альвеолярные клетки II типа (пневмоциты II типа).
Чем более недоношенным является младенец, тем меньше у него в момент рождения достаточного количества пневмоцитов II типа и, следовательно, чем более он недоношен, тем в большей степени ему недостает адекватной продукции сурфактанта.
Таким образом, заболеваемость неонатальным РДС обратно пропорциональна гестационному возрасту, и каждый недоношенный ребенок (гестационный возраст менее 38 недель) подвержен риску этого заболевания.
Неонатальный РДС широко распространен у крупных недоношенных детей (гестационный возраст менее 29 недель) и детей с низкой массой тела при рождении (менее 1,500 г).
Дефицит или отсутствие сурфактанта может быть вызвано или способствовать, помимо недоношенности, следующими факторами:
- мутации в одном или нескольких генах, кодирующих белки сурфактанта;
- синдром аспирации мекония;
- сепсис.
Генетические причины неонатального респираторного дистресс-синдрома
Очень редкие случаи являются наследственными и вызваны мутациями в генах.
- поверхностно-активного белка (SP-B и SP-C);
- комплекса, связывающего аденозинтрифосфат А3 (АВСА3).
Причины: незрелая паренхима легких.
Первоначально считалось, что единственной проблемой этого заболевания является снижение продукции сурфактанта незрелыми легкими недоношенных детей, тогда как более поздние исследования показали, что проблема, безусловно, более сложная.
Действительно, у недоношенного ребенка не только снижено количество сурфактанта, но и тот, который присутствует, также является незрелым и, следовательно, функционально менее эффективным.
Также неясно, насколько эффективно недоношенный ребенок может утилизировать имеющийся сурфактант.
Новорожденный с РДС также имеет незрелую легочную паренхиму со сниженной площадью поверхности альвеолярного газообмена, увеличенной толщиной альвеолярно-капиллярной мембраны, сниженной системой защиты легких, незрелой грудной стенкой и повышенной проницаемостью капилляров.
Любой острый эпизод асфиксии или снижение легочной перфузии способны нарушать выработку сурфактанта, делая его недостаточным и, таким образом, способствуя патогенезу РДС или усиливая его тяжесть.
Факторами риска неонатального РДС являются:
- преждевременные роды
- срок беременности 28 недель и менее;
- низкий вес при рождении (менее 1500 г, т.е. 1.5 кг)
- мужской пол;
- европеоидная раса;
- отец-диабетик;
- мать-диабетик;
- мать недоедает по умолчанию
- мать с многоплодной беременностью;
- мать злоупотребляет алкоголем и/или принимает наркотики;
- мать подверглась воздействию вируса краснухи;
- кесарево сечение без предшествующих родов;
- аспирация мекония (встречается преимущественно при переношенных или доношенных родах путем кесарева сечения);
- стойкая легочная гипертензия;
- транзиторное тахипноэ новорожденных (неонатальный синдром влажных легких);
- бронхо-легочная дисплазия;
- братья и сестры, родившиеся преждевременно и/или с пороками сердца.
Факторы, снижающие риск неонатального РДС (неонатального респираторного дистресс-синдрома):
- задержка роста плода
- преэклампсия;
- эклампсия;
- материнская гипертония;
- длительный разрыв плодных оболочек;
- использование матерью кортикостероидов.
патофизиология
Все новорожденные младенцы совершают свой первый дыхательный акт в тот момент, когда они появляются на свет.
Для этого новорожденные должны оказывать высокое давление при растяжении легких, поскольку при рождении легкие полностью спадаются.
В норме наличие сурфактанта позволяет снизить поверхностное натяжение в альвеолах, сохранить остаточную функциональную способность и, следовательно, начать вдох на благоприятном уровне легочной кривой давление-объем: при каждом акте остаточная функциональная способность увеличивается до тех пор, пока не достигнет нормальных значений.
Аномальное качество и количество сурфактанта у больного ребенка приводит к коллапсу альвеолярных структур и неравномерному распределению вентиляции.
По мере увеличения количества спавшихся альвеол младенец вынужден для адекватной вентиляции задействовать механизмы динамической компенсации, направленные на повышение давления в конце выдоха, тем самым препятствуя закрытию альвеол:
- повышает отрицательность внутриплеврального давления при вдохе;
- поддерживает тоническую активность инспираторных мышц во время выдоха, что делает грудную клетку более жесткой;
- увеличивает сопротивление дыхательных путей за счет приведения голосовых связок во время выдоха;
- увеличивает частоту дыхания и уменьшает время выдоха.
Растяжимость грудной стенки, которая является преимуществом во время родов, когда плод должен пройти через маточно-влагалищный канал, может быть недостатком, когда младенец с РДС вдыхает и пытается расширить нерастяжимые легкие, по сути, как отрицательное внутриплевральное давление, возникающее при попытке расширить нерастяжимые легкие, увеличивается, возникает тяга внутрь грудной клетки, и это явление ограничивает расширение легких.
Прогрессирующий ателектаз легкого также приводит к уменьшению функционального остаточного объема, что, в свою очередь, приводит к дальнейшему изменению газообмена в легких.
Следовательно, образуются гиалиновые мембраны, состоящие из белкового вещества, образующегося при повреждении легких, которые еще больше уменьшают растяжимость легких; наличие этих структур, таким образом, приводит к тому, что эта патологическая картина называется «болезнью гиалиновых мембран» - выражение, использовавшееся в прошлом для обозначения этого синдрома.
Белковая жидкость, выделяющаяся из поврежденных альвеол, вызывает инактивацию присутствующего дефицитного сурфактанта.
Присутствие этой жидкости и нарастание гипоксемии приводят к образованию обширных участков внутрилегочного шунта, которые еще больше подавляют активность сурфактанта.
Таким образом, возникает страшный порочный круг, характеризующийся непрерывной последовательностью
- снижение выработки поверхностно-активного вещества
- ателектаз;
- снижение растяжимости легких;
- измененное соотношение вентиляции/перфузии (V/P);
- гипоксемия;
- дальнейшее снижение производства поверхностно-активных веществ
- обострение ателектаза
Патологическая анатомия
Макроскопически легкие имеют нормальный размер, но более компактны, ателектатичны и имеют багрово-красный цвет, более похожий на цвет печени. Они также тяжелее обычных, настолько, что тонут при погружении в воду.
Микроскопически альвеолы развиты слабо и часто спадаются.
В случае ранней гибели младенца отмечают наличие в бронхиолах и альвеолярных ходах клеточного детрита, обусловленного некрозом альвеолярных пневмоцитов, которые в случае повышенной выживаемости заключаются в розоватые гиалиновые мембраны.
Эти оболочки покрывают дыхательные бронхиолы, альвеолярные ходы и реже альвеолы и состоят из фибриногена и фибрина (а также описанных выше некротических детритов).
Также можно отметить наличие слабой воспалительной реакции.
Наличие гиалиновых мембран является типичным компонентом болезни гиалиновых мембран легких, но они не встречаются у мертворожденных или младенцев, которые выживают всего несколько часов.
Если младенец выживает более 48 часов, начинают происходить репаративные явления: пролиферация альвеолярного эпителия и десквамация оболочек, фрагменты которых расходятся в дыхательные пути, где перевариваются или фагоцитируются тканевыми макрофагами.
Читайте также:
Обструктивное апноэ сна: что это такое и как его лечить
Обструктивное апноэ сна: симптомы и лечение обструктивного апноэ сна
Наша дыхательная система: виртуальный тур внутри нашего тела
Трахеостомия при интубации у пациентов с COVID-19: обзор современной клинической практики
FDA одобряет Recarbio для лечения внебольничных и связанных с вентилятором бактериальных пневмоний
Клинический обзор: острый респираторный дистресс-синдром
Стресс и дистресс во время беременности: как защитить мать и ребенка
Дыхательная недостаточность: каковы признаки дыхательной недостаточности у новорожденных?




