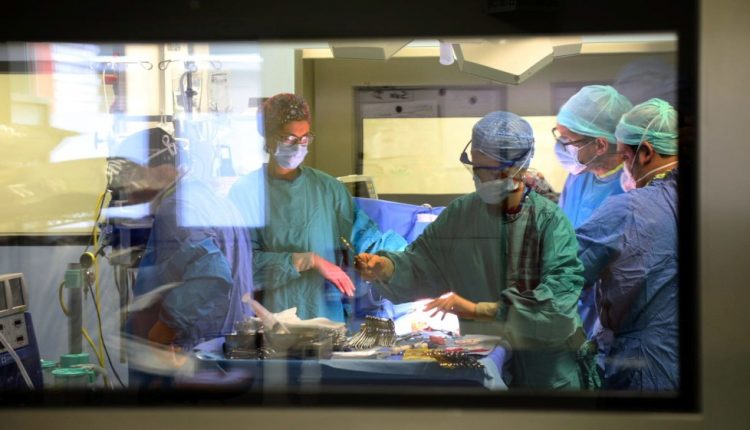
Trasplante de órganos: en qué consiste, cuáles son las etapas y qué depara el futuro
El trasplante de órganos es el procedimiento quirúrgico mediante el cual uno o más órganos enfermos (cuya funcionalidad ya no es recuperable) se reemplazan por uno o más órganos extraídos de un donante (cadáver o vivo)
Una operación que hunde sus raíces, conceptualmente, en la historia más antigua de la humanidad (de ella hablaron por primera vez los médicos chinos), es sin embargo una solución terapéutica muy reciente: los conocimientos que la hicieron posible (inmunología, estudio de antígenos…) fueron recién adquirida a principios del siglo XX.
A partir de 1950, el trasplante se convirtió en una opción consolidada en el tratamiento de aquellas patologías que conducen a la destrucción irreparable del órgano y, por tanto, a la muerte del paciente.
Pero el trasplante no es sólo la última perspectiva para aquellos cuya vida corre peligro: esta operación también permite mejorar la calidad de vida de aquellos pacientes que padecen enfermedades crónicas discapacitantes (por ejemplo, trasplante de riñón para pacientes dializados).
El futuro de los trasplantes aún está por esbozar, pero está muy claro en la mente de los científicos y médicos dedicados a la investigación: la implantación de órganos artificiales o tomados de animales modificados genéticamente (xenotrasplantes), la clonación y la implantación de células madre son solo algunos de las direcciones en las que se mueve el panorama científico mundial.
Cirugía de trasplante de órganos
La palabra 'trasplante' suele indicar, de forma reduccionista, la operación de sustitución de un órgano enfermo por uno sano.
En realidad, detrás de esta operación hay toda una organización y preparación que implica una extrema precisión y sincronización de personas e instrumentos.
La práctica de la operación difiere según el donante: si la extracción del órgano es de una persona viva, de hecho, es posible planificar la operación; lo cual obviamente no es factible si los órganos provienen de un donante cadavérico, quien murió por causas accidentales e imprevisibles.
Una vez que el comité médico ha obtenido el consentimiento de la familia y declara que se ha producido la muerte encefálica del potencial donante, comienza la evaluación de sus datos: compatibilidad con los posibles receptores en las listas de espera, historial médico, características inmunológicas, grupo sanguíneo, etc.
El trasplante de órganos se desarrolla a través de varias etapas.
FASE 1
Una persona con lesiones que podría ser donante (por ejemplo, un traumatismo craneoencefálico muy grave) ingresa en cuidados intensivos.
Un médico habla con la familia sobre la posibilidad de donar sus órganos; si están disponibles, se alerta inmediatamente al centro de coordinación, que es el responsable de informar al donante potencial e identificar al receptor potencial.
Mientras tanto, se valoran los datos del paciente donante: compatibilidad con los posibles receptores de la lista, historial médico, características inmunológicas. Comienza el período de observación de 6 horas, que es obligatorio antes de la certificación de muerte encefálica.
FASE 2
El equipo de explantación está activado y debe estar disponible en muy poco tiempo.
Los médicos suelen llegar al centro en helicóptero. Mientras tanto, en el hospital donde se realizará el trasplante, se llama al receptor para someterse a varios exámenes y evaluar su estado de salud.
También se realizan numerosos controles de los órganos a donar para evitar la transmisión de enfermedades infecciosas o tumores del donante al receptor.
FASE 3
Al final del período de observación, si todos los indicios apuntan a un diagnóstico de muerte cerebral irreversible, puede comenzar la explantación (aproximadamente 2 horas).
El receptor entra en el quirófano y se prepara para la operación. Se inicia ahora la administración de fármacos inmunosupresores para evitar que los linfocitos reconozcan el órgano como extraño y provoquen rechazo.
FASE 4
El órgano finalmente llega, sumergido en una solución especial para proteger sus células y transportado en un contenedor especial lleno de hielo para ralentizar su actividad celular.
Un equipo de médicos prepara al receptor, el otro se encarga de limpiar el órgano que se va a trasplantar.
FASE 5
Ahora puede comenzar el trasplante: los vasos sanguíneos están conectados, el sangrado está controlado.
PASO 6
El paciente sale del quirófano, pero sigue bajo anestesia, que se prolongará al menos otras 6 a 8 horas para que el nuevo órgano se acostumbre a la diferencia de temperatura entre el recipiente con el hielo y el cuerpo y, por supuesto, al propio órgano.
El paciente permanece conectado a la máquina para respirar.
PASO 7
El paciente se despierta en la unidad de cuidados intensivos; si su estado general es bueno, se le retira el respirador artificial.
Después de unos 4 días, vuelve a caminar y a comer.
Después de unos 10 días, podrá salir del hospital y vivir con su nuevo órgano.
Inicialmente, deberá regresar todos los días al hospital para controles inmunológicos; después de un año, podrá regresar una vez cada dos meses.
extracción de órganos
Una vez comprobada la muerte encefálica y obtenido el consentimiento de la familia (en caso de falta de voluntad expresa del donante), el potencial donante ya no es asistido por el respirador mecánico y los órganos pueden ser extraídos para trasplante en el mismo hospital que estableció la idoneidad. .
El equipo previamente alertado ingresa al quirófano para la operación de remoción.
Oponerse a la remoción nunca significa ayudar al paciente a tener una mejor atención; el cuidado, de hecho, termina en el momento en que se establece la muerte cerebral; oponerse a él, por lo tanto, solo significaría privar a otra persona de una vida mejor gracias a un nuevo órgano.
Hoy también gana terreno otro tipo de trasplante, el de personas vivas.
De hecho, ahora es posible tomar un lóbulo de riñón, hígado o pulmón para trasplante en personas particularmente en riesgo que no sobrevivirían en la lista de espera.
Suelen ser niños, tanto por la escasez de órganos pediátricos para trasplante como por el pequeño tamaño, lo que también hace que el donante no corra un riesgo demasiado alto.
Una vez tomados, los órganos requieren procedimientos especiales para preservarlos para el trasplante.
Existe, para cada órgano, un tiempo máximo de conservación, más allá del cual los tejidos, al no recibir más sangre, y por tanto oxígeno, entran en necrosis, es decir, sus células mueren, y por tanto quedan inutilizables.
Estos tiempos varían de un órgano a otro: corazón (4-6 horas), pulmón (4-6 horas), hígado (12-18 horas), riñón 48-72 horas, páncreas (12-24 horas).
Trasplante de órganos: rechazo
El rechazo es la reacción que tiene el organismo receptor hacia el órgano o tejido trasplantado.
De hecho, el sistema inmunitario del receptor reconoce el órgano como extraño y lo ataca como si fuera un patógeno.
Hay cuatro tipos de rechazo.
- rechazo hiperagudo: es el más rápido y ocurre a los pocos minutos u horas del trasplante;
- rechazo acelerado: a menudo ocurre en pacientes que ya han recibido un trasplante anterior y ocurre 3-4 días después de la operación;
- rechazo agudo: ocurre después de un período de tiempo que va de 5 a 90 días; los síntomas específicos son edema, fiebre y pérdida de función del órgano trasplantado;
- rechazo crónico: se desarrolla alrededor de 3 meses después del trasplante y puede causar daño tisular al nuevo órgano hasta el punto de perder su función.
Experimentar el rechazo del órgano trasplantado no significa necesariamente perderlo inevitablemente; por el contrario, el rechazo se trata con éxito si se actúa en un plazo razonable mediante el uso de fármacos inmunosupresores.
Los inmunosupresores que el médico prescriba después del trasplante ayudarán a que el órgano trasplantado no corra el riesgo de ser rechazado y se mantenga sano.
Dado que las células del sistema inmunológico son diferentes, los medicamentos recetados para la inmunosupresión también serán diferentes.
Indicaciones y contraindicaciones del trasplante de órganos
La indicación más grande y más inmediata para el trasplante es la falla irreversible de órganos vitales como riñones, hígado, pulmones, páncreas, pero también córneas, médula ósea, intestinos.
De hecho, en estos casos, el trasplante es el único tratamiento eficaz para asegurar la supervivencia.
Por lo tanto, cualquier condición patológica que impida el funcionamiento del órgano de tal manera que amenace la supervivencia del paciente debe considerarse una indicación de trasplante.
Cuidado postoperatorio
Después del trasplante, los receptores son admitidos durante los primeros días en una sala equipada para cuidados intensivos, donde se inicia la terapia inmunosupresora.
El paciente inmunodeprimido requiere aislamiento en habitaciones 'estériles', especialmente creadas para evitar cualquier tipo de contaminación del ambiente exterior.
El 'box' en el que se ingresa al receptor tras la operación de trasplante está completamente aislado del resto de la unidad de reanimación utilizada para la cirugía convencional.
La condición de aislamiento estricto persiste mientras el paciente supere la fase crítica posquirúrgica (normalmente 5-6 días), o en los casos en que se requiera terapia antirrechazo.
Visitas a pacientes trasplantados
En el período posquirúrgico inmediato, se permiten visitas a familiares cercanos siempre que estén vestidos adecuadamente (de acuerdo con los procedimientos de ingreso a la sala blanca).
Cada persona es admitida a la zona de filtrado de una en una y, por supuesto, no podrán ser admitidas personas con sospecha y/o evidencia de enfermedades infecciosas.
Desarrollos futuros
Los problemas más graves en medicina de trasplantes son, por un lado, el rechazo del órgano trasplantado y, por otro, la insuficiencia de los órganos donados frente a los necesarios.
En ambas direcciones, la investigación está experimentando con diversas soluciones para superar estos problemas.
En cuanto al rechazo, se intenta crear soluciones que consigan engañar al sistema inmunitario, reduciendo así la terapia inmunosupresora actualmente en uso, o que protejan al órgano trasplantado del ataque de los linfocitos T, que son los encargados de eliminar los agentes del exterior del organismo. .
En el otro frente, el de la escasez de órganos, se está experimentando con órganos artificiales, la ingeniería de tejidos o los xenotrasplantes que pueden sustituir a los órganos humanos.
La terapia génica
Mediante la terapia génica es posible ir al origen del problema y eliminar los defectos genéticos directamente en las células, tejidos u órganos afectados.
El gen sano se introduce directamente en el lugar afectado, donde comienza a producir aquellas sustancias que el cuerpo enfermo no puede producir por sí solo.
Sin embargo, la terapia génica aún está lejos de ser utilizada. Para poder transportar ADN extraño al núcleo de la célula, se necesitan 'vectores' especiales: virus que han perdido sus características infecciosas, pero que aún pueden atacar a las células y transmitirles su herencia genética.
Para evitar el rechazo, el órgano a trasplantar tendría que ser tratado en el laboratorio, transfiriéndole genes que lo hicieran capaz de defenderse del sistema inmunológico del receptor.
Ahora se conocen los genes, pero aún no se manejan con la precisión necesaria. El siguiente paso será buscar la combinación perfecta de genes que impida la acción de todos los mecanismos inmunológicos del receptor.
Ingeniería de tejidos
El objetivo de este tipo de terapia es encontrar una alternativa a los órganos humanos.
Ya ahora, los investigadores pueden producir tejidos como vasos sanguíneos, válvulas cardíacas, cartílagos y piel en el laboratorio.
Ha sido posible superar esta nueva frontera gracias a que las células tienden a agregarse para formar órganos y tejidos.
Las células madre
Las células madre son las células indiferenciadas que se encuentran en los embriones humanos una semana después de la fertilización.
También son las células "iniciales" a partir de las cuales se desarrollarán los tejidos y órganos del niño por nacer.
Su función es regular la renovación de las células sanguíneas (glóbulos rojos, Las células blancas de la sangre y plaquetas) y las del sistema inmunitario (linfocitos).
Hoy en día, se utilizan máquinas computarizadas, separadores, para recolectar estas células, lo que permite seleccionar las células necesarias. Los receptores de las células son pacientes que padecen enfermedades de la piel, enfermedades de la sangre o tumores sólidos.
Además del hecho de que las células madre aún son en gran parte desconocidas, también existe un problema ético: la recolección de células madre embrionarias implica la muerte del embrión.
Por eso se está perfeccionando la forma de cosechar células madre de adultos.
Clonación
La técnica de clonación permitiría eludir por completo el problema del rechazo de órganos.
Se trataría de introducir el núcleo de la célula del paciente, con toda su herencia genética, en la célula madre de un embrión humano o de un ovocito que antes no tenía núcleo propio.
Cultivadas in vitro en el laboratorio, estas células modificadas serían genéticamente idénticas a las del sistema inmunitario del paciente, que no las reconocería como extrañas.
Esta técnica no es una opción viable en la actualidad debido a que tanto la clonación, como la recolección de células madre y el uso indiscriminado de ovocitos están prohibidos por ley.
Xenotrasplante
El xenotrasplante, es decir, el trasplante de células, tejidos y órganos animales a humanos, parece ser la solución de futuro a la escasez de órganos para trasplante.
Los experimentos en este campo son numerosos y enfrentan problemas éticos, psicológicos y, por último, pero no menos importantes, inmunológicos.
De hecho, los pocos intentos que se han hecho (un hígado de cerdo y un corazón de babuino trasplantados a dos seres humanos diferentes) no han dado los resultados deseados.
La crisis de rechazo, de hecho, fue particularmente violenta e imposible de controlar.
Sin embargo, esta técnica podría ser realmente la solución a la escasez de órganos.
De hecho, lo que más se teme es el desarrollo de infecciones típicamente animales, transferidas al hombre a través de patógenos presentes en el órgano a trasplantar, lo que podría resultar desastroso.
Una posible alternativa a este hándicap podrían ser las modificaciones genéticas en los animales donantes; en la práctica, los animales serían criados en un ambiente estéril y modificados genéticamente para que sus órganos fueran más compatibles con el organismo del receptor.
Por el momento, sin embargo, se han alcanzado algunos hitos; estos son xenotrasplantes de células y no xenotrasplantes de órganos, como células de embrión de cerdo para el tratamiento de la enfermedad de Parkinson, células de médula de babuino trasplantadas en pacientes con sida terminal en un intento de recuperar el sistema inmunológico de los pacientes, o ínsulas de páncreas todavía de cerdos en la estimulación de la producción de insulina como terapia contra la diabetes.
Trasplante de órganos: órganos artificiales
Otra solución a la insuficiencia orgánica como el rechazo son los órganos artificiales.
El principal problema es la compatibilidad biológica; estos son, después de todo, órganos mecánicos que tienen que adaptarse a un organismo biológico.
La biocompatibilidad debe abarcar todas las características morfológicas, físicas, químicas y funcionales que sean capaces de asegurar la funcionalidad del órgano y, al mismo tiempo, su supervivencia sin riesgo de rechazo.
Son todas estas implicaciones las que hacen que la producción de órganos artificiales sea capaz de reemplazar completa y perfectamente a los órganos 'naturales' en sus funciones complejas.
Lea también:
Trasplante de órganos: diagnóstico y atención de pacientes en espera
¿Qué es el trasplante cardíaco? Una visión general
¿Cómo se realiza un trasplante de cara? - VIDEO



