X-seotud akrogigantism: uus uuring molekulaarsete mehhanismide tuvastamiseks
Acrogigantism: Humanitase teaduri dr Giampaolo Trivellini uurimisprojekt, mis sai alguse 2020. aasta märtsis ja mis viidi läbi tänu Marie Skłodowska Curie nimelise tegevus-individuaalstipendiumi 2018 võitmisele ja Telethoni fondi grandile (algas juunis 2021), on jõudnud esimene oluline järeldus
Nagu on märgitud 101. veebruaril 23 teadusajakirjas The American Journal of Human Genetics avaldatud uuringus „Duplikatsioonid häirivad kromatiini arhitektuuri ja juhivad ümber GPR2022-võimendiga side X-seotud akrogigantismi korral”, suutis dr Trivellin saada ülevaate patoloogilistest mehhanismidest. aluseks olev X-seotud akrogyantism (X-LAG).
X-LAG on haruldane geneetiline haigus, mida diagnoositakse praegu umbes 40 inimesel üle maailma, st 10%-l patsientidest, kellel on hüpofüüsi gigantism, mis on hüpofüüsi düsfunktsiooniga seotud patoloogia.
Akrogigantism: mis see on
X-seotud akrogigantismi kirjeldas esmakordselt 2014. aastal dr Trivellini töörühm ja see on seisund, mille põhjustab X-kromosoomis paiknev geneetiline defekt: täpsemalt geeni dubleerimine, mis sisaldab juhiseid GPR101-nimelise membraaniretseptori tootmiseks.
GPR101 dubleerimist seostatakse hüpofüüsi kasvajaga, mis põhjustab kasvuhormooni (GH) liigset sekretsiooni.
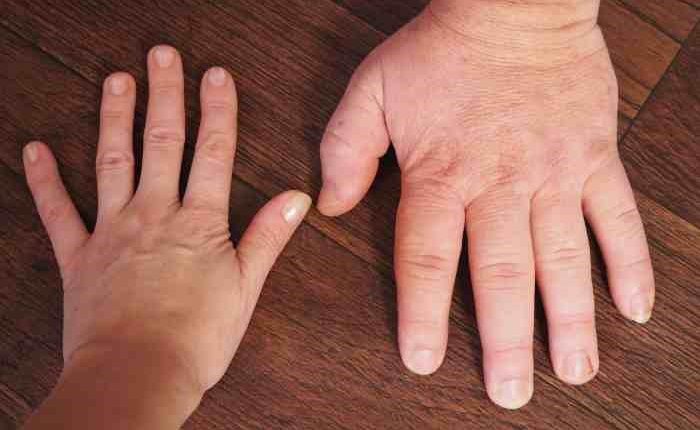
Akrogigantismi erinevate kliiniliste sümptomite hulgas on kõige ilmsem patsientide liigne kehakasv, mis ravimata jätmise korral ületab tavaliselt 2 meetrit.
Kuigi X-LAG-i ei saa ravida, saab seda praegu ravida multidistsiplinaarse lähenemisviisiga, mis hõlmab kirurgiat, meditsiinilist ravi ja harvemini kiiritusravi.
Akrogigantismi uurimistöö
Dr Trivellin ja tema uurimisrühm uurisid GPR101 geeni rolli ja molekulaarseid mehhanisme, mis põhjustavad selle märkimisväärset ekspressiooni hüpofüüsi kasvajates, mis olid seni teadmata.
Uuring näitas, et selle üleekspressiooni põhjus peitub kromatiini domeeni muutumises, milles geen asub.
See muutus on põhjustatud haigusega seotud dubleerimisest.
Meie DNA on jagatud kromatiini domeenideks ehk TAD-deks (topoloogilised seotud domeenid), mille ülesanne on hoida neis paiknevad geenid ülejäänud genoomist eraldatuna.
See lahterdamine tagab, et geeniekspressiooni võimendavate regulatoorsete elementide (võimendajate) toime piirdub ainult geenidega, mis asuvad samas kromatiini domeenis.
Erinevalt teistest geenidest, mida X-LAG patsientidel tavaliselt koos GPR101-ga dubleeritakse, on GPR101 ainus oma kromatiini domeenis, mis on teistest isoleeritud.
Patsientidel toimub geenide dubleerimisest tingitud kromatiini domeenide ümberkorraldamine, mille tulemuseks on uus kromatiini domeen, milles GPR101 geen ei ole enam eraldatud teiste geenide võimendajajärjestustest, vaid interakteerub nüüd nendega.
Just need uued patoloogilised koostoimed põhjustavad GPR101 märkimisväärset ekspressiooni patsientide kasvajates.
Acrogigantism, tulevikuväljavaated
Selle mehhanismi avastamine, mida Dr Trivellini uuringus esimest korda endokrinoloogias kirjeldas, avab edasisi uurimisvõimalusi nii hüpofüüsi haiguste kui ka muude endokriinsete häirete puhul, mis võivad areneda sarnaste patoloogiliste mehhanismide kaudu.
Teadmine, mis määrab GPR101 retseptori üleekspressiooni, mis on kasvuhormooni ületootmiseni viivate rakusiseste signaalide kaskaadi promootor, on gigantismist mõjutatud patsientide uues terapeutilises perspektiivis ülioluline.
See on esimene samm edasise ravi suunas, mis spetsiifiliselt pärsib GPR101-ga interakteeruvaid võimendusjärjestusi akrogigantismiga patsientidel: GPR101 geeni üleekspressiooni väljalülitamine vähendab kasvuhormooni liigset sekretsiooni ja sellega kaasnevaid kurnavaid sümptomeid.
Loe ka:
COVID-19 Downi sündroomiga inimestel: suremus kuni kümme korda suurem. Uuring ISS-ist
Downi sündroom ja COVID-19, uuringud Yale'i ülikoolis
Downi sündroomiga lapsed: Alzheimeri tõve varase arengu tunnused veres



