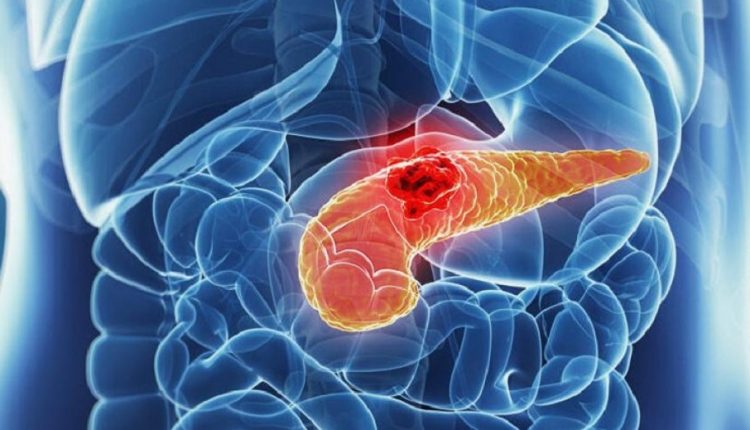
Bukspyttkjertel: forebygging og behandling av kreft i bukspyttkjertelen
Det finnes flere andre typer kreft i bukspyttkjertelen, men adenokarsinom er den vanligste neoplasmen i bukspyttkjertelen
Det er en sykdom som har sin opprinnelse i kanalene som bærer fordøyelsesenzymer produsert av bukspyttkjertelen, og årsakene til disse er fortsatt ukjente.
Det dannes som et resultat av akkumulering av bukspyttkjertelceller som har gjennomgått en genetisk endring som får dem til å formere seg ukontrollert, uten noen gang å dø, og som vokser og sprer seg raskt.
Dette er grunnen til at det er en vanskelig neoplasma å diagnostisere på et tidlig stadium.
Typer av eksokrine svulster i bukspyttkjertelen
Omtrent 80 % av eksokrine svulster i bukspyttkjertelen er adenokarsinomer i det ductale epitelet, og bare 2 % er godartede.
Det er noen svært sjeldne eksokrine svulster som gigantisk cellekarsinom, adenosquamous carcinoma, microglandulært adenokarsinom, mucinøst karsinom, cystadenocarcinoma, papillært cystisk karsinom, cystadenocarcinoma og acinarcelle cystadenocarcinoma, og til slutt forbinder primært lymfom bukspyttkjertelvev.
Cystiske svulster utgjør mindre enn 5 % av alle bukspyttkjertelsvulster (tidlig mucinøst cystadenom og cystadenocarcinoma), mens intraduktale og mucinøse svulster (både godartede og ondartede) vanligvis forekommer som en cystisk dilatasjon av bukspyttkjertelens kanalsystem.
Endokrine svulster, som initieres av celle i bukspyttkjertelen, kan være funksjonelt inaktive, godartet eller ondartet, og inkluderer insulinomer, glukagonomer og gastrinomer.
Omtrent 40 % av endokrine svulster i bukspyttkjertelen er ikke-funksjonelle, og av disse er opptil 90 % ondartede
Det er flere syndromer som inkluderer neoplasmer assosiert med svulster i bukspyttkjertelen.
Av disse er den mest kjente multippel endokrin neoplasi (MEN) type 1 (parathyreoideahyperplasi, endokrine bukspyttkjertelsvulster og hypofysesvulster), og gastrinomer og insulinomer er hyppigst representert her.
Disse variasjonene i tumorfunksjon påvirker diagnose og behandlingsstrategier.
Klinisk strategi og behandling for kreft i bukspyttkjertelen
Når diagnosen kreft i bukspyttkjertelen stilles, er det nødvendig å vurdere om den er mottakelig for radikal kirurgisk reseksjon.
En bukspyttkjertelsvulst i generelle termer er definert som resektabel når den kan fjernes uten å etterlate neoplastiske rester (R0), uopererbar når den ikke kan resekeres fullstendig (R1-2) eller borderline når radikalitet er tvilsom preoperativt og man må stole på neoadjuvante terapier eller direkte på kirurgisk evaluering under operasjonen.
Dessverre er bare rundt 20 % av pasientene med kreft i bukspyttkjertelen på diagnosetidspunktet radikalt resektable.
Derfor er det avgjørende å definere tumorstadie i henhold til TNM-systemet (AJCC) så nøyaktig som mulig for å unngå unødvendige inngrep.
AJCC iscenesettelse av en kreft i bukspyttkjertelen er som følger:
Tumor (T)
TX – Primærsvulst kan ikke vurderes
T0 – Ingen tegn på primær svulst
Tis – Karsinom in situ
T1 – Svulst begrenset til bukspyttkjertelen, 2 cm eller mindre i maksimal størrelse
T2 – Svulst begrenset til bukspyttkjertelen, større enn 2 cm i største dimensjon
T3 – Tumor strekker seg utover bukspyttkjertelen (f.eks. tolvfingertarmen, gallegang, portal eller mesenterisk vene superior), men involverer ikke cøliakiaksen eller mesenterial arterie superior
T4 – Tumor involverer cøliakiaksen eller mesenteriske arterier
Regionale lymfeknuter (N)
NX – Regionale lymfeknuter kan ikke vurderes
N0 – Ingen regionale lymfeknutemetastaser
N1 – Regionale lymfeknutemetastaser
Fjernmetastaser (M)
MX – Fjernmetastaser kan ikke vurderes
M0 – Ingen fjernmetastaser
M1 – Fjernmetastaser
Stadiegrupperingen for kreft i bukspyttkjertelen er som følger:
Trinn 0 – Tis, N0, M0
Trinn IA – T1, N0, M0
Trinn IB – T2, N0, M0
Trinn IIA – T3, N0, M0
Trinn IIB – T1-3, N1, M0
Trinn III – T4, Enhver N, M0
Trinn IV – Enhver T, Enhver N, M1
Ved første presentasjon har bare 20 % av pasientene stadium I sykdom, 40 % har lokalt avansert sykdom og 40 % har metastatisk sykdom til lymfeknuter eller fjerne steder.
Generelt sett er T1- og T2-stadier begrenset til bukspyttkjertelparenkymet, mens T3-lesjoner invaderer lokale strukturer som tolvfingertarmen, gallegangen og/eller store peripankreatiske vener og T4-lesjoner invaderer omkringliggende organer (f.eks. mage, tykktarm, lever) eller store arterier slik som de øvre mesenteriske eller cøliakiarteriene.
Preoperativ staging laparoskopi
Noen sentre anbefaler å utføre en iscenesettelse laparoskopi før du fortsetter til laparatomi.
Hensikten med laparoskopisk stadieinndeling er å unngå å utsette pasienter med lever- eller peritoneale metastaser som ikke er synlige med vanlige radiologiske metoder for unødvendig kirurgi.
En slik undersøkelse er imidlertid hensiktsmessig når disse situasjonene er tilstede:
- CA 19-9 nivå > 150 U/ml
- Lavt volum ascites
- Svulster i kroppen av bukspyttkjertelen
- Borderline resektable svulster
- Svulststørrelse > 3 cm
- Vanlig gallegang lymfadenopati
- Terapi og behandling av kreft i bukspyttkjertelen i operasjonsformer
Det er en rimelig konsensus i litteraturen om at kirurgi, når det er radikalt mulig, er hovedbehandlingsmetoden for kreft i bukspyttkjertelen.
Imidlertid er det en viktig rolle for kjemoterapi og/eller strålebehandling i en adjuvant eller neoadjuvant setting og i behandlingen av pasienter med ikke-opererbar sykdom.
Generelt utelukker ekstrapankreatisk sykdom kurativ reseksjon, og kirurgisk behandling kan i beste fall være lindrende.
Generelt betraktes vaskulær infiltrasjon som en kontraindikasjon for bukspyttkjertelreseksjon, selv om invasjon av den mesenteriske eller øvre portalvenen i dag ikke lenger er en absolutt kontraindikasjon, faktisk kan sistnevnte fjernes og rekonstrueres (i tillegg er venen i mange tilfeller bare komprimert og ikke infiltrert) ved bruk av den indre halsvenen, venen saphenus eller miltvenen.
Vurderingen av infiltrasjonen av de øvre mesenteriske, cøliaki- og hepatiske arteriene er derimot annerledes, da de utvilsomt representerer en absolutt kontraindikasjon for radikal reseksjon.
I denne sammenhengen må den kirurgiske tilnærmingen tilpasses tumorstedet og derfor vil duodenocephalopankreasektomi (DCP), med eller uten pylorussparing, total pankreasektomi (PT) og distal pankreasektomi (PD) vurderes.
Disse prosedyrene, som krever at kirurger med erfaring i denne typen operasjoner utfører, har en forekomst av komplikasjoner og preoperativ risiko som må være kjent og diskuteres med pasienten før operasjonen kan fortsette.
Pankreaskreftretningslinjene til European Society of Medical Oncology (ESMO) indikerer at fullstendig kirurgisk reseksjon er den eneste potensielt kurative behandlingen tilgjengelig; Imidlertid er 5-års total overlevelse bare 10-20 %, og langtidsoverlevelsen hos pasienter med lymfeknutespredning er ekstremt dårlig.
ESMO-anbefalingene inkluderer følgende
Optimal symptomatisk behandling spiller en nøkkelrolle i behandlingen av metastatisk sykdom; Pasienter kan trenge drenasje- eller bypassoperasjoner for obstruktiv gulsott eller gastrisk obstruksjon.
Rollen til kjemoterapi er begrenset. Gemcitabin har vært assosiert med en liten overlevelsesfordel sammenlignet med bolus 5-fluorouracil.
Hos pasienter med lokalt avansert ikke-opererbar kreft i bukspyttkjertelen, har lokal ablasjon blitt utforsket som et terapeutisk alternativ. En systematisk gjennomgang konkluderte med at følgende strategier ser ut til å være gjennomførbare og trygge:
- Radiofrekvensablasjon (RFA)
- Irreversibel elektroporasjon
- Stereotaktisk strålebehandling (SBRT)
- Høyintensitetsfokusert ultralyd (HIFU)
- Jod-125
- Jod-125-kryokirurgi
- Fotodynamisk terapi
- Mikrobølgeablasjon
- Mange av disse ablative teknikkene har vist seg å gi smertelindring og forbedret overlevelse.
For eksempel er medial overlevelse på opptil 25.6 måneder rapportert med RFA og 24.0 måneder med SBRT. Lovende resultater på livskvalitet er rapportert for SBRT.
De andre prosedyrene har vist lovende resultater i enkelte anlegg, men har fortsatt lavt opptak.
Kjemoterapi for kreft i bukspyttkjertelen
Det finnes i dag ingen behandlingsprotokoller som gir garantier for suksess på dette området.
Det antas at hos pasienter med metastatisk sykdom kan kombinasjonen av Gemcitabin og Erlotinib gi signifikant høyere median overlevelse og 1-års overlevelse enn bruk av Gemcitabin alene.
Noen studier indikerer at Gemcitabin-Capecitabin-kombinasjonen er et av standard førstelinjealternativer ved lokalt avansert og metastatisk kreft i bukspyttkjertelen, mens andre studier har vist at FOLFIRINOX-kombinasjonen (leucovorin pluss 5-lfuourouracil [LV5-FU] pluss oksaliplatin pluss irinotekan ) er i stand til å fremme en median overlevelse på 11.1 måneder sammenlignet med 6.8 måneder i gruppen Gemcitabin alene.
Det er foreløpig ingen enhetlig aksepterte og avtalte protokoller.
Adjuverende terapi
Flere studier har antydet muligheten for at kjemoterapi, med eller uten strålebehandling, kan forbedre median overlevelse betydelig etter kirurgisk reseksjon av operabel sykdom.
Disse studiene er ikke definitive og er ikke allment akseptert for å rettferdiggjøre kjemo-strålebehandling for adjuvant terapi.
Neoadjuvant terapi
Bruken av kjemoterapi og/eller strålebehandling i neoadjuvant setting er også fortsatt en kilde til kontrovers.
Begrunnelsen for bruk av neoadjuvant terapi inkluderer påstandene om at:
- kreft i bukspyttkjertelen er en systemisk sykdom og må behandles systematisk fra første stund;
- pasienter er i stand til å tolerere de toksiske effektene av kjemoterapi lettere før de gjennomgår større bukspyttkjertelreseksjon etterpå;
- svulsten kan krympe i størrelse med neoadjuvant terapi og reseksjon kan være mindre kompleks, noe som fører til bedre total overlevelse.
Problemet er at det fortsatt ikke er noen endelig enighet om hvilke behandlingsprotokoller som skal brukes i denne kliniske settingen.
Duodenocephalopancreasektomi (Whipples DCP-prosedyre)
Denne operasjonen utføres hos pasienter som har en neoplasma i hodet av bukspyttkjertelen, Vaters papilla eller terminal koledok eller tolvfingertarmen.
Operasjonen innebærer tradisjonelt fjerning av bukspyttkjertelhodet, tolvfingertarmen, galleblæren og antrum av magen, med kirurgisk drenering av den distale bukspyttkjertelkanalen og gallesystemet, vanligvis utført ved anastomose med en digiunal løkke (galle-fordøyelsesanastomose).
DCP har vist seg å ha en total dødelighet på 6.6 % og en sykelighet på 25 %.
De alvorligste komplikasjonene er anastomotiske fistler, forsinket mageutløp og fordøyelsesblødning.
Hos pasienter med gulsott foreslår mange forfattere bruk av galledrenasje (endoskopisk eller transhepatisk) plassert preoperativt.
For å være effektiv må imidlertid biliær drenering opprettholdes i tilstrekkelig tid for å normalisere eller nesten normalisere bilirubinnivået (ca. 20 dager).
Men denne løsningen, i tillegg til å forsinke operasjonen, disponerer for risiko for infeksjon i galleveiene, som igjen er forbundet med økt risiko for postoperative infeksjonskomplikasjoner og sårinfeksjon, og finner av disse grunner ikke overbeviste støttespillere i flertallet av forfatterne.
Whipples standardoperasjon kan modifiseres ved å unngå reseksjon av gastrisk antrum ved å bevare pylorus.
Denne modifikasjonen har blitt foreslått for å forbedre ernæringsstatusen til pasienten (reservoarfunksjon av magesekken), men kan være belastet av en økt risiko for å bremse magetømming (fjerning av duodenum-gastrisk innervasjon).
Fra et onkologisk synspunkt er det ingen forskjeller mellom de to prosedyrene.
Bukspyttkjertelkreft, retningslinjene til European Society of Medical Oncology gir følgende anbefalinger
- kirurgisk reseksjon med radikal hensikt er den eneste potensielt kurative behandlingen tilgjengelig. Imidlertid er 5-års total overlevelse bare 10-20%; Langtidsoverlevelsen i svulster med positive lymfeknuter er ekstremt dårlig.
- Optimal symptomatisk behandling spiller en nøkkelrolle i behandlingen av metastatisk sykdom; disse pasientene kan trenge drenasje- eller bypassoperasjoner for obstruktiv gulsott eller obstruksjon av gastrisk utløp.
- Rollen til kjemoterapi er begrenset; Gemcitabin alene eller i kombinasjon med andre legemidler har vært assosiert med en liten overlevelsesfordel.
Distal pankreatektomi (PD)
Denne prosedyren har en lavere dødelighet enn Whipples standardprosedyre, på 3.5 %, men bruken ved kurativ reseksjon er fortsatt begrenset.
PD er effektiv og teknisk mindre kompleks enn DCP i distalt lokaliserte svulster.
Dessverre blir masser som ligger i dette området diagnostisert mye senere og er derfor vanligvis lett inoperable på grunn av vaskulær trombose eller gastrisk eller intestinal infiltrasjon.
Prosedyren innebærer isolering av den distale delen av bukspyttkjertelen som inneholder svulsten, etterfulgt av reseksjon av det segmentet med eller uten milten, med suturering av den distale bukspyttkjertelkanalen.
De viktigste komplikasjonene for PD er bukspyttkjertelfistel, blødning og en abscess.
Det er viktig å plassere tilstrekkelig drenering av området involvert i den kirurgiske handlingen.
Total pankreasektomi (PT)
Selv om denne prosedyren er den minst ofte utførte, kan den fortsatt være et verdifullt verktøy i kirurgisk behandling av kreft i bukspyttkjertelen, spesielt i tilfeller der svulsten involverer hals av bukspyttkjertelen eller det er mistanke om at svulsten har metastasert langs kanalen til Wirsung.
Dødeligheten er rundt 8 % og sykeligheten er lavere (faktisk er det ingen risiko for bukspyttkjertelfistler eller anastomotisk dehiscens), men det resulterer i en definitiv postoperativ total diabetestilstand som ikke alltid er lett å behandle.
Palliativ terapi for kreft i bukspyttkjertelen
Smerte
Hos pasienter som ikke er mottakelige for kirurgisk reseksjon, er det nødvendig å tilby terapi for å forebygge og behandle de mest betydelige og invalidiserende symptomene på sykdommen.
Smertelindring er avgjørende i denne sammenhengen.
Bruk av narkotiske analgetika bør foreslås tidlig og i passende doser i kombinasjon med trisykliske antidepressiva eller antiemetika for å forsterke deres smertestillende effekt.
Hos pasienter hvor narkotika er utilstrekkelig, bør andre tilnærminger vurderes, slik som cøliaki ganglion nevrolyse, som kan gi betydelig langsiktig smertelindring.
Dette kan utføres transthorakalt eller transabdominalt ved bruk av intervensjonsradiologi eller anestesiologi, transgastrisk ved bruk av en finnålsinjeksjon under ultralyd- eller CT-veiledning.
Eller intraoperativt under evaluering av pasientens reseksjonspotensial.
Strålebehandling for kreft i bukspyttkjertelen kan lindre smerte, men det påvirker ikke pasientens overlevelse.
Noen pasienter kan oppleve smerte på grunn av obstruksjon av bukspyttkjertelen eller gallegangene, spesielt hvis smertene forverres betydelig etter å ha spist.
Disse pasientene kan ha nytte av endoskopisk dekompresjon med bukspyttkjerteldrenasje plassert endoskopisk retrograd.
Gulsott
Obstruktiv gulsott er en alvorlig komplikasjon for pasienten med kreft i bukspyttkjertelen i hodet, da det resulterer i uhåndterlig kløe, som forårsaker alvorlige skrapeskader.
Løsningen av dette symptomet kan oppnås ved plassering av en intern (transtumoral) galledren introdusert endoskopisk retrograd, intern ekstern (med en ekstern og en intern transtumoral gren) eller ekstern (når svulsten ikke kan overføres) ved hjelp av en transkutan radiologisk prosedyre.
Metallekspansjonsproteser er dyrere og permanente, har lengre åpningstid og er å foretrekke hos pasienter med forventet levetid på mer enn 3 måneder.
Plast er mye billigere og må vanligvis skiftes hver 3-4 måned og brukes fortrinnsvis til pasienter med kortere forventet levetid.
Hos pasienter i god allmenntilstand kan disse prosedyrene også utføres kirurgisk, ved hjelp av en bilio-digestiv anastomose (for å omgå neoplasma i bukspyttkjertelhodet), en gastro-digiunal anastomose for å unngå duodenal obstruksjon og sikre ernæringsmessig kontinuitet, og cøliaki nevrolyse til forhindre smerter i bukspyttkjertelen.
Kosthold for pasienter med kreft i bukspyttkjertelen
Som med de fleste pasienter med avansert kreft, er pasienter med bukspyttkjertelkreft ofte anorektiske.
Farmakologisk appetittstimulering er vanligvis mislykket, men kan prøves.
Pasienter kan ha en viss grad av malabsorpsjon sekundært til eksokrin pankreasinsuffisiens forårsaket av kreft som blokkerer bukspyttkjertelkanalen.
Pasienter med malabsorpsjonsdiaré og vekttap kan ha nytte av tilskudd av pankreasenzym.
Deres diaré kan også forbedres ved å unngå dietter med høyt fett eller høyt proteininnhold.
Forebygging av kreft i bukspyttkjertelen
Epidemiologiske data viser at røyking er årsaken til ca. 30 % av bukspyttkjertelsvulstene.
Spesifikke tobakkskreftfremkallende stoffer er metylnitrosaminer, nitrosonornikotiner, polysykliske aromatiske hydrokarboner og aromatiske aminer.
Ulike studier har vist at sigarettrøykere utvikler kreft i bukspyttkjertelen 3.3 til 9.5 år tidligere enn ikke-røykere.
Sigarettrøykere har 70 % høyere risiko for bukspyttkjertelsvulster enn ikke-røykere.
Sigaretter med røykfilter reduserer ikke risikoen for kreft.
Å ikke røyke eller slutte å røyke for godt bør betraktes som en betydelig kreftforebyggende faktor.
Pasienter med alkoholrelatert kronisk pankreatitt, hvis de samtidig er langtidsrøykere, har også økt risiko for kreft i bukspyttkjertelen og spiserøret.
Kirurgisk fjerning av kreft i bukspyttkjertelen kan også ha et forebyggende aspekt hos pasienter med kronisk alkoholisk pankreatitt.
Siden ca. 10 % av alle svulster i bukspyttkjertelen utvikler seg på grunnlag av kronisk arvelig pankreatitt og en familiær genetisk disposisjon, er regelmessige screeningsundersøkelser (EUS, CT-skanning, MR) annethvert til fjerde år under diskusjon for disse risikogruppene fra 40 år. .
Det er ennå ikke gitt bevis for effektiviteten av screeningundersøkelser.
Erfaring med bruk av profylaktisk reseksjon ved høyrisiko kreft i bukspyttkjertelen er imidlertid så langt kun tilgjengelig for et lite antall pasienter.
Pasienter med cystiske neoplasmer i bukspyttkjertelen utvikler ofte bukspyttkjertelkreft på lang sikt
Med IPMN-svulster (Intraductal Papillary Mucinous Pancreatic Neoplasms) observeres ondartet transformasjon til ductal pancreascancer hos omtrent 60 % -70 % av pasientene.
Ved IPMN-neoplasi er karsinomet hovedsakelig lokalisert i hodet av bukspyttkjertelen.
Mucinøse cystiske neoplasmer viser ondartet transformasjon i omtrent 20 % av tilfellene.
Selv om den økte kunnskapen om sekvensielle genetiske mutasjoner i cystisk neoplasi i bukspyttkjertelen ennå ikke tillater pålitelig risikoprediksjon, har erfaring vist at kirurgisk fjerning er indisert for cystiske neoplasmer på mer enn 2 eller 3 cm, spesielt når diagnosen er kjent (IPMN, MCN og serøst cystisk adenom).
Ved mange av disse sykdommene er fullstendig fjerning av cystiske neoplasmer en kreftforebyggingsstrategi og utføres nå uten kirurgisk dødelighet i spesialiserte sentre.
Fullstendig fjerning av en cystisk svulst (IPMN, MCN) tilbyr pasienter en kur mot cystisk neoplasma og lindrer dem fra frykten for å utvikle kreft i bukspyttkjertelen.
Les også:
Emergency Live enda mer...Live: Last ned den nye gratisappen til avisen din for iOS og Android
Svangerskapsdiabetes, hva det er og hvordan det skal håndteres
Kreft i bukspyttkjertelen, en ny farmakologisk tilnærming for å redusere utviklingen
Hva er pankreatitt og hva er symptomene?
Nyrestein: Hva de er, hvordan behandle dem
Akutt pankreatitt: årsaker, symptomer, diagnose og behandling



