Fekální bakterioterapie: fekální transplantace pro Clostridium difficile, kolitidu a Crohnovu chorobu
Fekální bakterioterapie, také známá jako fekální transplantace nebo fekální transfuze nebo infuze lidských probiotik (HPI) nebo transplantace fekálního mikrobiomu, je nefarmakologická léčebná léčba v experimentální fázi, která se s určitou účinností používá u subjektů trpících pseudomembranózní kolitidou. bakterie Clostridium difficile (nedávno přejmenovaná na „Clostridium difficile“); nebo dokonce v případech ulcerózní kolitidy refrakterní na běžné terapie
Cílem této inovativní terapie je obnovit mikrobiální ekologii a homeostázu tlustého střeva opětovným zavedením zdravé (vyvážené) lidské mikroflóry, odebrané z trusu zdravého dárce nebo v některých případech z trusu dříve „darovaného“ stejným subjektem ( homotransfuze nebo autologní obnova gastrointestinální flóry – ARGF).
Teoretické zdůvodnění této terapeutické techniky lze nalézt v nejpokročilejším výzkumu využití probiotik a studiích o mikrobiomu, což je soubor mikroorganismů: bakterie, archeobakterie, houby, viry, přítomné ve specifickém prostředí (v tomto v případě fekálního prostředí).
Je dobře známo, jak dobrá mikrobiální ekologie dokáže odrazit přemnožení patogenních organismů.
V tlustém střevě se odhaduje, že existuje 500 až asi 1000 různých druhů bakterií s celkovým počtem 1013 bakterií.
Ve skutečnosti by měl být mikrobiom považován za biologickou entitu jako takovou, která je symbiontem s hostitelským organismem.
Bakteriální komplex nebo mikrobiom působí při udržování homeostázy hostitelského organismu; tato mikrobiální flóra je po opětovném zavedení do těla relativně neškodná.
O úloze mikrobiomu není mnoho známo, je však známo, že mnoho býložravých a nebýložravých druhů zvířat má koprofágní návyky, pravděpodobně kvůli dvojitému trávicímu cyklu (dvojité trávení).
Fekální transplantace: hlavní výhodou fekální bakterioterapie je snížení rizika indukce antibiotické rezistence u vysoce patogenních bakterií
Dalšími výhodami jsou relativně nízké náklady, nepotřebnost léků a dobrá účinnost (bude však potvrzena – avšak – rozsáhlejšími studiemi) pro léčbu případů rezistence na antibiotika.
Metoda je však stále považována za léčbu „poslední záchrany“ pro její větší invazivitu ve srovnání s konvenční léčbou antibiotiky a potenciální rizika přenosu infekce (bakterie, viry, priony, střevní paraziti).
Přestože jsou zkušenosti s fekální bakterioterapií stále omezené, publikované výsledky tohoto postupu ukazují, že více než 80 pacientů prokázalo průměrnou úspěšnost přes 90 %
Fekální bakterioterapie je technologicky nenáročný, snadno proveditelný postup, který dokáže přerušit cykly opakovaného užívání antibiotik, což následně snižuje riziko v poslední době narůstajícího výskytu antibiotické rezistence.
Má také potenciál ušetřit náklady ve srovnání s opakovaným podáváním antibiotik s nutnými hospitalizacemi.
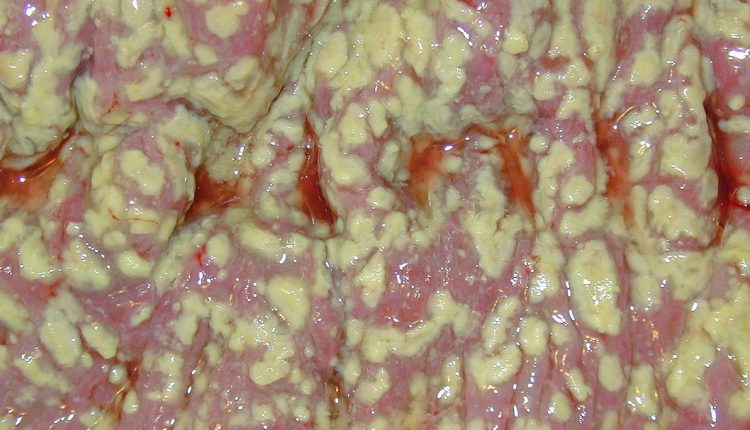
Pseudomembranózní kolitida
Význam jako patogen Clostridium difficile (CDI) je pevně stanoven již od roku 1978, ale význam této techniky v léčbě pseudomembranózní kolitidy pramení také ze skutečnosti, že se její epidemiologie v poslední době změnila, což pro klinické lékaře představuje vážné diagnostické a terapeutické problémy. .
Míra infekce (CDI) se zdvojnásobila z 31/100,000 1996 v roce 61 na 100,000/2003 XNUMX v roce XNUMX.
V posledních letech se závažnost a mortalita infekce C. difficile CDI zvyšuje, což bylo přičítáno novému virulentnímu kmeni C. difficile známému jako kmen severoamerické pulsní gelové elektroforézy typu 1 (NAP-1) resp. také PFGE typ BI/NAP1 ribotyp 027.
Jedinečnost kmene NAP-1 spočívá ve zvýšené produkci toxinů A a B a v produkci binárních toxinů a odolnosti vůči fluorochinolonu.
Hypervirulentní kmeny NAP1 C. difficile jsou zodpovědné za většinu nedávných nozokomiálních ohnisek a rozšířené používání fluorochinolonových antibiotik mohlo usnadnit selektivní proliferaci tohoto kmene.
Kmen NAP1 také pravděpodobněji způsobí těžkou fulminantní kolitidu charakterizovanou výraznou leukocytózou, akutním selháním ledvin, hemodynamickou nestabilitou a toxickým megakolonem.
C. difficile se stala nejčastější bakteriální příčinou nozokomiálních průjmů.
Infekce Clostridium difficile způsobuje CDAD (Clostridium difficile Associated Disease) nebo vzácněji pseudomembranózní kolitidu, což je závažný zdravotní stav způsobující významnou morbiditu a mortalitu, zejména u pacientů podstupujících léčbu antibiotiky nebo u pacientů s rakovinou podstupujících transplantaci kmenových buněk nebo dokonce u pacientů podstupujících radioterapii .
Zvýšená frekvence infekcí hypervirulentními kmeny C. difficile vedla při konvenční léčbě metronidazolem a vankomycinem ke komplikacím a terapeutickým selháním.
Ačkoli s omezenými klinickými zkušenostmi, fekální bakterioterapie předběžně prokázala vysokou míru klinického vyléčení, dosud však chybí randomizované klinické studie pro tento terapeutický přístup.
Ulcerózní kolitida
U ulcerózní kolitidy nebyl dosud nalezen žádný patogen.
Ale účinnost fekální bakterioterapie v tomto případě by naznačovala, že příčina ulcerózní kolitidy může být způsobena předchozí infekcí patogenem, který zůstal neznámý.
Počáteční infekce mohla u těchto pacientů pravděpodobně vymizet přirozeně; ale někdy může nerovnováha ve střevní flóře tlustého střeva vést k zánětlivému vzplanutí (což by vysvětlovalo cyklickou a opakující se povahu tohoto onemocnění).
Zdá se, že tento cyklus je, alespoň v mnoha případech, přerušen rekolonizací pacientova tlustého střeva bakteriálním komplexem (probiotikem) odebraným ze zdravého střeva (heterograft).
Někteří lékaři se domnívají, že tato léčba prováděná u zdravých jedinců je bezpečná a mnoho pacientů by z této inovativní terapie mohlo mít prospěch.
Studie z května 2011 potvrdila dobrou ochotu pacientů a rodičů dětí s ulcerózní kolitidou přijmout tuto léčbu, jakmile překonali počáteční nechuť k metodě.
V roce 2013 další výzkum potvrdil validitu terapie prospektivní pilotní studií na deseti subjektech ve věku 7-21 let.
Tato studie prokazuje snášenlivost a účinnost léčby fekální transplantací u ulcerózní kolitidy; ve skutečnosti u sedmi subjektů došlo ke klinické remisi během jednoho týdne a šest z devíti si udrželo klinickou remisi po jednom měsíci.
Transplantace stolice, další onemocnění studovaná pro fekální bakterioterapii
Tato technika je v současné době studována u subjektů s Parkinsonovou chorobou, diabetem, obezitou, syndromem dráždivého tračníku, chronickým zánětlivým onemocněním střev, roztroušenou sklerózou, idiopatickou trombocytopenickou purpurou, Crohnovou chorobou, inzulinovou rezistencí a syndromem chronické únavy.
Klasický postup
Obvykle se používá výkaly blízkého zdravého příbuzného pacienta po vyšetření a vyloučení přítomnosti nakažlivých bakterií nebo virů nebo parazitů, jako jsou: Salmonella, virus hepatitidy atd.
Vzorek stolice je po odběru zpracován a připraven v klinické laboratoři ve formě tekuté suspenze, která je následně instilována do horní části gastrointestinálního traktu nazogastrickou sondou, která vede až do úrovně céka.
Procedura někdy zahrnuje 5-10 dní léčby klystýry, vyrobenými s lidskou mikroflórou ze stolice zdravého dárce; většina pacientů se uzdraví již po jednom ošetření.
Nejlepší volbou dárce je blízký příbuzný, který byl testován na širokou škálu bakteriálních a parazitárních agens.
Klystýry se připravují a podávají v nemocničním prostředí, aby byla zajištěna veškerá potřebná péče.
Infuzi probiotik lze také provést nazogastrickou sondou, která dopraví bakterie přímo do tenkého střeva.
Tyto dvě metody lze kombinovat pro dosažení nejlepšího výsledku.
Pravidelné kontroly by měly být prováděny do jednoho roku po zákroku.
ARGF (autologní obnova gastrointestinální flóry)
Modifikovanou formou fekální bakterioterapie, která se v současnosti vyvíjí, je autologní obnova gastrointestinální flóry – (ARGF).
Tato metoda je bezpečnější, efektivnější a snadněji se aplikuje.
Autologní (vlastní) vzorek stolice si pacient před léčbou poskytne a uchová v chladničce.
Pokud se u pacienta následně rozvine patologie C. difficile, vzorek se extrahuje fyziologickým roztokem a přefiltruje. Filtrát se lyofilizuje a výsledná pevná látka se uzavře do gastrorezistentních kapslí.
Podávání kapslí obnovuje pacientovu vlastní střevní flóru, což je užitečné v boji proti jakékoli infekci C. difficile, která se mohla objevit.
Tento postup odstraňuje rizika klasické fekální bakterioterapie, kdy by případná infekce mohla být na pacienta přenesena dárcem, a také odpadá nutnost podávat vzorek stolice do duodena žaludeční sondou.
Účinnost
Účinnost metody v prevenci recidiv pseudomembranózní kolitidy se odhaduje kolem 90 %.
Studie z prosince 2011 potvrzuje tato data prokazující 92% účinnost metody v prevenci průjmu nebo další recidivy u skupiny 26 pacientů s recidivujícími infekcemi C. difficile.
Finská studie z roku 2011 poukazuje na to, že antibiotická léčba recidivujících infekcí Clostridium difficile (CDI) vede u 50 % pacientů k recidivám.
Použití fekální transplantace během kolonoskopického testu po intestinálním preparátu polyethylenglykolem (výplach) vedlo k vyřešení 89 % případů recidivující pseudomembranózní kolitidy při jednoročním sledování, se zdůrazněním, že léčené případy byly způsobeny zvláště virulentní kmen C. difficile (typ 027).
Také v prosinci 2011 prokázala revize 317 pacientů 92% účinnost metody a také málo vedlejších účinků.
V roce 2015 byla publikována srovnávací studie s vankomycinem prokazující nadřazenost bakteriální fekální terapie nad tímto antibiotikem.
Přečtěte si také
Nouzové živě ještě více…Živě: Stáhněte si novou bezplatnou aplikaci vašich novin pro IOS a Android
Kolitida: Příznaky, léčba a co jíst
Ulcerózní kolitida: Příčiny, příznaky a léčba
Bakterie střeva dítěte mohou předpovídat budoucí obezitu
Transplantace fekální mikrobioty (transplantace stolice): K čemu slouží a jak se provádí?
Sant'Orsola v Bologni (Itálie) otevírá novou lékařskou hranici s transplantací mikrobioty
Microbiota, role „brány“, která chrání mozek před objeveným střevním zánětem
Jaké jsou rozdíly mezi divertikulitidou a divertikulózou?
Co je to jehlová biopsie prsu?
Kolonoskopie: Nejnovější techniky a různé typy
Dysbióza a hydrokolonová terapie: Jak obnovit střevní pohodu
Kapslová endoskopie: Co to je a jak se provádí
Kolonoskopie: Co to je, kdy to udělat, příprava a rizika
Colon Wash: Co to je, k čemu to je a kdy je to třeba udělat
Rektosigmoidoskopie a kolonoskopie: co jsou a kdy se provádějí
Ulcerózní kolitida: Jaké jsou typické příznaky onemocnění střev?
Wales 'Úmrtnost na chirurgii střev' vyšší, než se očekávalo '
Syndrom dráždivého tračníku (IBS): Benigní stav, který je třeba udržet pod kontrolou
Střevní infekce: Jak se nakazí infekce Dientamoeba Fragilis?
Studie nalezla souvislost mezi rakovinou tlustého střeva a užíváním antibiotik
Kolonoskopie: Efektivnější a udržitelnější s umělou inteligencí
Kolorektální resekce: V jakých případech je nutné odstranění tlustého střeva
Gastroskopie: K čemu je vyšetření a jak se provádí
Gastroezofageální reflux: Příznaky, diagnostika a léčba
Endoskopická polypektomie: Co to je, kdy se provádí
Zvedání rovné nohy: Nový manévr k diagnostice refluxní choroby jícnu
Gastroenterologie: Endoskopická léčba gastroezofageálního refluxu
Ezofagitida: Příznaky, diagnostika a léčba
Gastroezofageální reflux: Příčiny a náprava
Gastroskopie: co to je a k čemu slouží
Divertikulární nemoc tlustého střeva: Diagnostika a léčba divertikulózy tlustého střeva
Gastroezofageální refluxní choroba (GERD): Příznaky, diagnostika a léčba
Divertikula: Jaké jsou příznaky divertikulitidy a jak ji léčit
Syndrom dráždivého tračníku (IBS): Benigní stav, který je třeba udržet pod kontrolou
Gastroezofageální reflux: příčiny, příznaky, testy pro diagnostiku a léčbu
Non-Hodgkinův lymfom: Příznaky, diagnostika a léčba heterogenní skupiny nádorů
Helicobacter pylori: Jak jej rozpoznat a léčit



