هیپرکلسترولمی خانوادگی: چیست و چگونه می توان آن را درمان کرد
هایپرکلسترولمی خانوادگی ، یک بیماری نادر ژنتیکی است که باعث عواقب جدی سلامتی (به عنوان مثال حمله قلبی و سکته مغزی) می شود که به اقدامات مهار مناسب با داروهای مناسب و سبک زندگی مناسب نیاز دارد.
هیپرکلسترولمی یعنی چه؟ و خانوادگی یعنی چی؟
هایپرکلسترولمی یک بیماری بالینی است که با کلسترول بیش از حد در خون مشخص می شود.
کلسترول جز component لیپیدها است ، که معمولاً با رژیم غذایی مصرف می شود اما می تواند توسط بدن نیز تولید شود.
کلسترول برای زندگی بسیار مهم است زیرا برای تشکیل غشاهای سلولی (برای اطمینان از عملکرد آنها) استفاده می شود ، از سلولهای عصبی و اعصاب جمجمه محافظت می کند.
کلسترول همچنین برای سنتز مولکولهای دیگر نیز مورد استفاده قرار می گیرد ، سه مورد از آنها اسیدهای صفراوی (مهم برای هضم غذا) ، برخی هورمونها و ویتامین D هستند.
فقط در صورت وجود بالاتر از این الزامات می تواند آسیب جدی وارد کند.
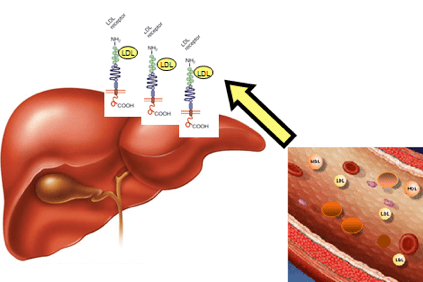
در مورد هایپرکلسترولمی ، کلسترول به صورت لیپوپروتئین های سبک (LDL) ، مواد خاص چربی و پروتئین ، که کلسترول بد نامیده می شود ، در خون تجمع می یابد که باعث ایجاد پلاک در دیواره شریان (پلاک های آترواسکلروتیک) می شود.
این اتفاق زمانی می افتد که بیماران سطح کلسترول بالایی دارند که نمی توانند آن را از طریق مکانیسم های فیزیولوژیکی کبد از بین ببرند.
تجمع LDL در خون در نهایت منجر به تشکیل آتروما (انسداد فیزیکی جریان خون طبیعی) می شود که می تواند منجر به عواقب جدی تری مانند آنژین ، حمله قلبی ، سکته مغزی ، بلکه در سایر اندام ها مانند مغز ، کلیه ها ، ریه ها و خود کبد.
افزایش کلسترولمی در هنگام انتقال به فرزندان آشنا است
این به دلیل اصلاح ژنی است که حاوی اطلاعاتی برای ساخت پروتئین کبدی است ، گیرنده LDLR (LDLR) که LDL را تشخیص می دهد ، آن را از جریان خون خارج کرده و به سلول های کبدی منتقل می کند و سپس آن را حذف می کند. این تغییر ژن باعث تجمع LDL در خون می شود.
تا به امروز ، بیش از 600 تغییر در ژن LDL شناخته شده است که باعث افزایش کلسترولمی در خانواده می شود.
همچنین ، افراد مبتلا به این اختلال می توانند تغییراتی در ژن های دیگر درگیر در متابولیسم های لیپوپروتئین مانند ژن APOB (آپوپروتئین B در LDL) و ژن PCSK9 (پروتئین تخریب کننده گیرنده های LDL) ایجاد کنند.
اگرچه شناخته شده است كه تجمع كلسترول می تواند مضر باشد ، اما تخمین زده می شود كه تا یك سوم حملات قلبی كه قبل از 40 سالگی اتفاق می افتد به دلیل كاهش کلسترولمی خانوادگی تشخیص داده نشده یا به طور نامناسب است.
شایعتر هیپرکلسترولمی چند عاملی است که به علت عوامل محیطی ایجاد می شود (رژیم غذایی با چربی بالا ، به خصوص اگر با عدم تحرک بدنی همراه باشد) حتی در صورت وجود عوامل مستعد کننده ژنتیکی.
اشکالی که هایپرکلسترولمی خانوادگی خود را نشان می دهد
این بیماری می تواند خود را به 2 شکل مختلف بروز دهد: یک نوع کمتر جدی (هتروزیگوت ، 1 مورد در هر 500 نفر) و یک بیماری جدی تر (هموزیگوت ، 1 مورد در هر 1,000,000،1,2،XNUMX فرد) XNUMX،XNUMX.
شکل هتروزیگوت اغلب بدون علامت است و فقط بر اساس سطح کلسترول خون تشخیص داده می شود.
کبد برای از بین بردن LDL تلاش می کند زیرا گیرنده های LDL در تعداد ناکافی تولید می شوند ، در نتیجه در مقایسه با مقادیر طبیعی ، سطح خون 2 یا 3 برابر افزایش می یابد.
این فرم می تواند منجر به افزایش خطر بیماری های قلبی عروقی در بزرگسالی شود.
شکل هموزیگوت با شروع بیماری های قلبی عروقی حتی در سنین جوانی و وجود تجمع مشخص چربی مانند گزانتوم (گره های مایل به زرد در انگشتان دست و تاندون آشیل) و گزانتالاسما (صفحات زردرنگ پلک ها و اطراف) مشخص می شود. چشمها).
نقص ژنتیکی از هر دو والدین به ارث می رسد و خطر حمله قلبی در صورت عدم وجود درمان در حال حاضر در حدود 15-20 سالگی مشاهده شده است.
در حقیقت ، در این شرایط ، کبد قادر به متابولیسم لیپوپروتئین های باقی مانده در خون نیست ، و سپس تجمع یافته منجر به اختلالات عملکردی که در بالا توضیح داده شد ، می شود و وضعیتی ناسازگار با زندگی ایجاد می کند.
احتمال انتقال بیماری به کودکان چقدر است؟
از آنجایی که هر یک از ما دو نسخه از هر ژن داریم که هر یک از والدین به ارث رسیده است ، هنگامی که یک نسخه تغییر یافته و یک نسخه سالم به ارث ببریم ، فرم هتروزیگوت خواهیم داشت.
برعکس ، اگر هر دو نسخه از ژن بیمار را از هر دو والد به ارث ببریم ، فرم هموزیگوت خواهیم داشت. باید گفت که این فرم بسیار نادر است زیرا فقط زمانی اتفاق می افتد که والدین هر دو ژن عامل بیماری را داشته باشند و بنابراین هر یک از آنها می توانند نسخه ای از همان تغییر ژن را منتقل کنند.
به هیپرکلسترولمیای خانوادگی آسیب شناسی هتروزیگوت گفته می شود که در موارد نادری که دو نوع مختلف تغییر ژن به ارث می رسد ، یکی از هر یک از والدین است.
كودكانی كه در معرض خطر ابتلا به این بیماری هستند باید زود تشخیص داده و درمان شوند. امروزه تشخیص بیماری از طریق آزمایش های ژنتیکی که به دنبال خطا (تغییر ژن) روی ژن های LDLR ، ApoB و PCSK9 است امکان پذیر است.
بنابراین فقط اشکال هایپرکلسترولمی خانوادگی قابل انتقال است.
با این حال ، اشکال چند عاملی که عمدتا به دلیل سبک زندگی نادرست (تجمع کلسترول با رژیم غذایی) رخ می دهد ، همچنین می تواند با یک استعداد ژنتیکی مشخص شود.
در حقیقت ، این افراد ممکن است نقایص ژنتیکی داشته باشند که توانایی بدن در جبران کافی چربی های اضافی در رژیم غذایی را به خطر بیندازد.
به عنوان مثال ، هنگامی که کبد از کلسترول همراه با غذا اشباع می شود ، تولید گیرنده هایی که LDL گردش خون را جذب می کنند ممکن است سرکوب شود.
وضعیت بسیار شبیه وضعیتی است که در طی هایپرکلسترولمی خانوادگی اتفاق می افتد اگرچه شدت آن کمتر است.
در این حالت ، غلظت کلسترول تام در خون بالاتر از حد طبیعی است و معمولاً بین 240 تا 350 میلی گرم در دسی لیتر است در مقایسه با میزان طبیعی که معمولاً در حدود 200 - 240 میلی گرم در دسی لیتر تنظیم می شود.
یک کنجکاوی: این بیماری ممکن است طی قرن ها منتقل شده باشد
مشاهده دقیق نقاشی معروف مونالیزا این احتمال را نشان می دهد که مونالیزا در سن جوانی از پرکلسترولمی خانوادگی رنج برده است.
در واقع ، لئوناردو همچنین با وفاداری رسوبات چربی معمولاً در دست و نزدیک چشم (که اکنون به عنوان گزانتوما و گزانتالاسما شناخته می شوند) را به تصویر می کشد که وجود آسیب شناسی را با قطعیت نشان می دهد.
اگر این واقعیت داشته باشد ، نشان داده شده است که هایپرکلسترولمیای خانوادگی بیماری است که در طول قرن ها حفظ شده است (موردی که از اوایل سال 1500 به ثبت رسیده است).
چه امکاناتی برای درمان این بیماری وجود دارد؟
امکان درمان بیماری به شدت آن بستگی دارد. همچنین ، عوامل خطر (رژیم غذایی ، استعمال دخانیات ، سن ، خانواده و سابقه شخصی کلسترول خون ، وجود بیماری های دیگر) می توانند تصویر کلی بیماری را بدتر کنند.
برای درمان هایپرکلسترولمی خانوادگی می توان از داروهای نسل جدید استفاده کرد ، اما در عین حال لازم است که با اصلاح سبک زندگی مناسب اقدام شود.
در موارد شدت متوسط (هایپرکلسترولمی خانوادگی هتروزیگوت) ، داروی درمانی مبتنی بر استاتین (مهارکننده های سنتز کلسترول که باعث افزایش سنتز گیرنده LDLR می شوند) و ترکیب با ازتیمیب (مهارکننده های جذب کلسترول) یا داروهای بازدارنده PCSK9 (یعنی مهارکننده های پروتئین PCSK9 که نقش آنها این است گیرنده های کبدی را که LDLR را از بین می برند از بین می برد) فعالیت کپی سالم ژن LDLR را بهبود می بخشد و تجمع کلسترول را در خون کاهش می دهد.
اسید بمپدوئیک که اخیراً مورد تأیید قرار گرفته است ، دارویی است که با مهار آنزیم ATP سیترات لیاز ، مولکولی که در روند سنتز کلسترول درون زا نقش دارد ، در کبد عمل می کند.
این مکانیسم عملکرد به ما اجازه می دهد تا بر اساس میزان کلسترول تولید شده ، بالادست از محل عمل استاتین ها عمل کرده و بیان گیرنده های LDL را تحریک کنیم تا سنتز کاهش یافته را جبران کند.
برخلاف استاتین ها ، اسید بمپدوییک در عضله اسکلتی فعال نیست ، که احتمال وقوع حوادث ناخواسته معمولی در مورد استاتین ها را کاهش می دهد.
این دارو همچنین می تواند با ازتیمایب با اثرات مطلوب همراه باشد.
هیپرکلسترولمی خانوادگی هموزیگوت تا همین اواخر یک بیماری لاعلاج در نظر گرفته می شد.
درمان مبتنی بر استاتین در این آسیب شناسی مثر نیست. در حقیقت ، استاتین هایی که بر اساس مکانیسم هایی که منجر به تولید کلسترول درون زا می شوند عمل می کنند ، نمی توانند سنتز گیرنده های LDL را تحریک کنند.
برای از بین بردن کلسترول LDL از بدن این بیماران ، پلاسمافرز ، روشی است که فیلتر کردن خون با از بین بردن چربی ها را امکان پذیر می کند ، همان کاری که در هنگام کار نکردن کلیه با دیالیز انجام می شود.
با این حال ، این یک روش تهاجمی است و تأثیر منفی بر کیفیت زندگی بیماران دارد.
آخرین تحقیق در مورد هایپرکلسترولمی خانوادگی
در سال های اخیر ، تحقیقات منجر به تولید داروهای خاص نیز برای فرم هموزیگوت هایپرکلسترولمی خانوادگی شده است ، که انتظار و کیفیت زندگی بیماران مبتلا به آن را بسیار بهبود می بخشد.
به عنوان مثال ، داروی لومیتاپید (به صورت خوراکی مصرف می شود) منجر به کاهش قابل توجه سطح LDL-کلسترول پلاسما در این بیماران می شود.
لومیتاپید یک پروتئین حمل و نقل تری گلیسیرید میکروزومی (MTP) را مهار می کند که اجازه می دهد این لیپیدها را همراه با آپوپروتئین B100 در VLDL های نوپای ترکیب کند.
در نتیجه ، آپوپروتئین B100 و LDL حتی در بیمارانی که بیماری باعث فقدان گیرنده LDL شده است ، کاهش می یابد.
داروی نسل جدید دیگر میپومرسن است ، یک الیگونوکلئوتید ضد حس است که قادر به تخریب آپوپروتئین های B100 است که در تشکیل LDL شرکت می کنند ، بنابراین تعداد دومی را کاهش می دهد.
Evolocumab و alirocumab دو آنتی بادی مونوکلونال هستند که از فعالیت پروتئین PCSK9 در خون جلوگیری می کنند.
با این حال ، برای تأثیرگذاری این دو دارو ، حداقل قسمت کوچکی از گیرنده های LDL باید وجود داشته و کار کنند.
از جمله داروهایی که هنوز در حال پیشرفت بالینی هستند ، گنجاندن داروی بیولوژیکی (اصطلاحاً siRNA) است که رونویسی DNA و سنتز پروتئین PCSK9 در کبد را مسدود می کند.
نتایج مثبت اخیراً با evinacumab ، یک بازدارنده آنتی بادی مونوکلونال پروتئین مشابه آنژیوپویتین 3 (ANGPTL3) ، مولکولی سنتز شده توسط کبد که نقش آن افزایش کلسترول-LLDL و سطح تری گلیسیرید است و از تخریب آنها جلوگیری می کند ، به دست آمده است.
این داروی جدید همچنین در بیمارانی که گیرنده LDL کار نمی کند ، اثربخشی نشان داده است.
اخیراً برخی از تلاشها برای درک اینكه آیا ژن درمانی ، با ورود ژن سالم به DNA بیمار ، مثر است نیز انجام شده است 5.
از این لیست درمان های احتمالی برای هایپرکلسترولمی خانوادگی ، می توان فهمید که چه مقدار تحقیق برای ارائه راه حل برای این بیماران که اگرچه نادر هستند ، اما به این بیماری جدی مبتلا هستند ، انجام می شود و خطر عواقب مرگبار را کاهش می دهد.
با این حال ، مثل همیشه که در مورد داروهای جدید اتفاق می افتد ، استفاده از یک کلمه احتیاط در استفاده مزمن آنها خوب است زیرا دانش در مورد عوارض جانبی احتمالی آنها فقط با تجربه (دارویی و هوشیاری) واضح تر خواهد بود ، بنابراین استفاده از آنها در کودکان باید به دقت ارزیابی شود ، البته با هدف نهایی ارائه این امکان برای زندگی "طبیعی" به این بیماران "کوچک".
منابع کتابشناختی و سیتوگرافیک مقاله مربوط به پرکلسترولمی خانوادگی
1 دستورالعمل ESC / EAS 2019 برای مدیریت اختلالات چربی خون: اصلاح چربی برای کاهش خطر قلب و عروق نویسندگان / اعضای گروه ویژه کمیته دستورالعمل های ESC (CPG) ؛ انجمن های ملی قلب ESC. تصلب شرایین نوامبر 2019 ؛ 290: 140-205. doi: 10.1016 / j.atherosclerosis.2019.08.014.
2 دیس لیپیدمیای نادر ، از فنوتیپ به ژنوتیپ تا مدیریت: بیانیه اجماع کارگروه انجمن آترواسکلروز اروپا. Hegele RA ، Borén J ، Ginsberg HN ، Arca M ، Averna M ، Binder CJ ، Calabresi L ، Chapman MJ ، Cuchel M ، von Eckardstein A ، Frikke-Schmidt R ، Gaudet D ، Hovingh GK ، Kronenberg F ، Lütjohann D ، Parhofer KG ، Raal FJ ، Ray KK ، Remaley AT ، Stock JK ، Stroes ES ، Tokgözoğlu L ، Catapano AL. دیابت Lancet Endocrinol. 2020 ژانویه ؛ 8 (1): 50-67. doi: 10.1016 / S2213-8587 (19) 30264-5.
3 لیپوپروتئین (الف) کاهش-از لیپوپروتئین آفرزیس به رویکرد آنیسنس الیگونوکلئوتید. Greco MF ، Sirtori CR ، Corsini A ، Ezhov M ، Sampietro T ، Ruscica MJ Clin Med. 2020 ژوئیه 3 ؛ 9 (7): 2103. doi: 10.3390 / jcm9072103.
4 درمان کاهش دهنده کلسترول LDL. Pirillo A ، Norata GD ، Catapano AL. Handb Exp Pharmacol. 2020 آوریل 30. doi: 10.1007 / 164_2020_361.
5 مروری بر درمان های مبتنی بر ژن و سلول برای هایپرکلسترولمی خانوادگی. حاجی قاسمی اس ، مهدوی گورابی A ، بیانکونی V ، پیررو M ، Banach M ، احمدی تفتی H ، Reiner Ž ، صاحبکار A.Pharmacol Res. مه 2019 ؛ 143: 119-132. doi: 10.1016 / j.phrs.2019.03.016.



