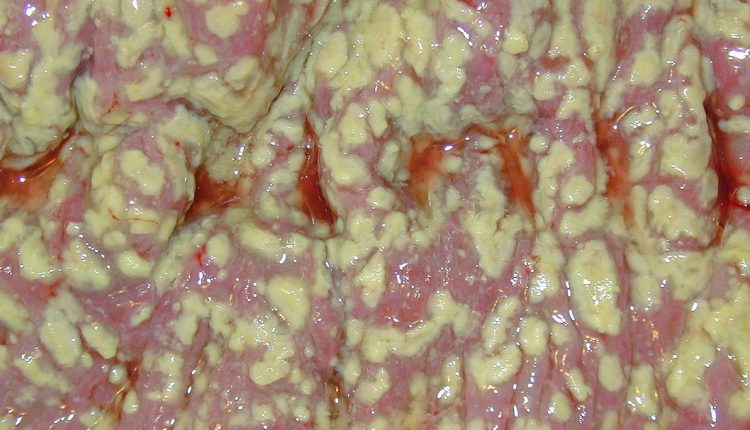
Fäkale Bakteriotherapie: Fäkaltransplantation bei Clostridium difficile, Colitis und Morbus Crohn
Die fäkale Bakteriotherapie, auch bekannt als fäkale Transplantation oder fäkale Transfusion oder Infusion menschlicher Probiotika (HPI) oder fäkale Mikrobiomtransplantation, ist eine nicht-pharmakologische medizinische Behandlung in einer experimentellen Phase, die mit einiger Wirksamkeit bei Patienten angewendet wird, die an pseudomembranöser Kolitis leiden, die durch die Clostridium difficile-Bakterium (kürzlich umbenannt in „Clostridium difficile“); oder sogar in Fällen von Colitis ulcerosa, die auf herkömmliche Therapien nicht ansprechen
Das Ziel dieser innovativen Therapie ist die Wiederherstellung der mikrobiellen Ökologie und Homöostase des Dickdarms durch die Wiedereinführung einer gesunden (ausgewogenen) menschlichen Mikrobiota, die aus dem Kot eines gesunden Spenders oder in bestimmten Fällen aus Kot stammt, der zuvor von demselben Probanden „gespendet“ wurde ( Homotransfusion oder autologe Wiederherstellung der Magen-Darm-Flora – ARGF).
Die theoretische Begründung für diese therapeutische Technik findet sich in der fortschrittlichsten Forschung zur Verwendung von Probiotika und Studien zum Mikrobiom, das die Gruppe von Mikroorganismen ist: Bakterien, Archäobakterien, Pilze, Viren, die in einer bestimmten Umgebung vorhanden sind (in diesem Fall die fäkale Umgebung).
Es ist bekannt, wie eine gute mikrobielle Ökologie das übermäßige Wachstum pathogener Organismen abwehren kann.
Im Dickdarm gibt es schätzungsweise 500 bis etwa 1000 verschiedene Bakterienarten mit insgesamt 1013 Bakterien.
Tatsächlich sollte das Mikrobiom als eigenständige biologische Einheit betrachtet werden, die mit dem Wirtsorganismus symbiont.
Der Bakterienkomplex oder das Mikrobiom wirkt bei der Aufrechterhaltung der Homöostase des Wirtsorganismus; Diese mikrobielle Flora ist relativ harmlos, wenn sie wieder in den Körper eingeführt wird.
Über die Rolle des Mikrobioms ist nicht viel bekannt, jedoch ist bekannt, dass viele pflanzenfressende und nicht pflanzenfressende Tierarten koprophage Gewohnheiten haben, wahrscheinlich aufgrund eines doppelten Verdauungszyklus (Doppelverdauung).
Stuhltransplantation: Der Hauptvorteil der fäkalen Bakteriotherapie besteht darin, das Risiko einer Antibiotikaresistenz bei hochpathogenen Bakterien zu verringern
Weitere Vorteile sind relativ niedrige Kosten, keine Notwendigkeit von Medikamenten und eine gute Wirksamkeit (die jedoch durch größere Studien bestätigt werden muss) für die Behandlung von Fällen, in denen Antibiotikaresistenzen bestehen.
Die Methode gilt jedoch aufgrund ihrer größeren Invasivität im Vergleich zur herkömmlichen Behandlung mit Antibiotika und der potenziellen Risiken einer Infektionsübertragung (Bakterien, Viren, Prionen, Darmparasiten) immer noch als Behandlung der „letzten Instanz“.
Obwohl die Erfahrung mit der fäkalen Bakteriotherapie noch begrenzt ist, zeigen veröffentlichte Ergebnisse zu diesem Verfahren, dass über 80 Patienten eine durchschnittliche Erfolgsrate von über 90 % gezeigt haben.
Die fäkale Bakteriotherapie ist ein einfach durchzuführendes Low-Tech-Verfahren, das Zyklen der wiederholten Antibiotikaanwendung durchbrechen kann, was wiederum das Risiko des in letzter Zeit zunehmenden Auftretens von Antibiotikaresistenzen verringert.
Im Vergleich zu wiederholten Antibiotika-Gaben mit den notwendigen Krankenhausaufenthalten hat sie zudem das Potenzial, Kosten einzusparen.
Pseudomembranöse Kolitis
Die Bedeutung von Clostridium difficile (CDI) als Erreger ist seit 1978 fest etabliert, aber die Bedeutung dieser Technik bei der Behandlung von pseudomembranöser Kolitis rührt auch von der Tatsache her, dass sich ihre Epidemiologie in letzter Zeit geändert hat, was Kliniker vor ernsthafte diagnostische und therapeutische Probleme stellt .
Die Infektionsraten (CDI) haben sich von 31/100,000 im Jahr 1996 auf 61/100,000 im Jahr 2003 verdoppelt.
In den letzten Jahren hat die Schwere und Sterblichkeit einer C. difficile-CDI-Infektion zugenommen, und dies wurde einem neuen virulenten Stamm von C. difficile zugeschrieben, der als North American Pulsed-field gel electrophoresis type 1 (NAP-1)-Stamm oder bekannt ist auch PFGE Typ BI/NAP1 Ribotyp 027.
Die Einzigartigkeit des NAP-1-Stammes liegt in seiner erhöhten Produktion der Toxine A und B und seiner binären Toxinproduktion und Resistenz gegen Fluorchinolon.
Hypervirulente NAP1-Stämme von C. difficile sind für die Mehrzahl der jüngsten nosokomialen Ausbrüche verantwortlich, und die weit verbreitete Verwendung von Fluorchinolon-Antibiotika könnte die selektive Proliferation dieses Stamms erleichtert haben.
Der NAP1-Stamm verursacht auch eher schwere, fulminante Colitis, die durch ausgeprägte Leukozytose, akutes Nierenversagen, hämodynamische Instabilität und toxisches Megakolon gekennzeichnet ist.
C. difficile ist zur häufigsten bakteriellen Ursache nosokomialer Durchfälle geworden.
Eine Clostridium-difficile-Infektion verursacht CDAD (Clostridium difficile Associated Disease) oder seltener eine pseudomembranöse Kolitis, eine schwerwiegende Erkrankung, die zu erheblicher Morbidität und Mortalität führt, insbesondere bei Patienten, die sich einer Behandlung mit Antibiotika unterziehen, oder Krebspatienten, die sich einer Stammzelltransplantation unterziehen, oder sogar bei Patienten, die sich einer Strahlentherapie unterziehen .
Die erhöhte Häufigkeit von Infektionen durch hypervirulente C. difficile-Stämme hat zu Komplikationen und Therapieversagen bei der konventionellen Behandlung mit Metronidazol und Vancomycin geführt.
Trotz begrenzter klinischer Erfahrung hat sich vorläufig gezeigt, dass die fäkale Bakteriotherapie hohe klinische Heilungsraten bietet, jedoch fehlen bis heute randomisierte klinische Studien für diesen therapeutischen Ansatz.
Colitis ulcerosa
Bei Colitis ulcerosa wurde bisher kein Erreger gefunden.
Die Wirksamkeit der fäkalen Bakteriotherapie in diesem Fall würde jedoch darauf hindeuten, dass die Ursache der Colitis ulcerosa möglicherweise auf einer früheren Infektion mit einem unbekannt gebliebenen Erreger beruht.
In der Tat kann die anfängliche Infektion bei diesen Patienten wahrscheinlich auf natürliche Weise abgeklungen sein; aber manchmal kann ein Ungleichgewicht in der Darmflora des Dickdarms zu einem entzündlichen Aufflammen führen (was die zyklische und wiederkehrende Natur dieser Krankheit erklären würde).
Dieser Zyklus scheint zumindest in vielen Fällen unterbrochen zu werden, indem der Dickdarm des Patienten mit einem Bakterienkomplex (Probiotikum) aus einem gesunden Darm (Heterotransplantat) erneut besiedelt wird.
Einige Ärzte glauben, dass diese Behandlung bei gesunden Probanden sicher ist und viele Patienten von dieser innovativen Therapie profitieren könnten.
Eine Studie im Mai 2011 bestätigte die gute Bereitschaft von Patienten und Eltern von Kindern mit Colitis ulcerosa, diese Behandlung zu akzeptieren, nachdem sie ihre anfängliche Abneigung gegen die Methode überwunden hatten.
Im Jahr 2013 bestätigte eine weitere Studie die Gültigkeit der Therapie mit einer prospektiven Pilotstudie an zehn Probanden im Alter von 7 bis 21 Jahren.
Diese Studie zeigt die Verträglichkeit und Wirksamkeit der Stuhltransplantationstherapie bei Colitis ulcerosa; Tatsächlich kam es bei sieben Probanden innerhalb einer Woche zu einer klinischen Remission, und sechs von neun behielten die klinische Remission nach einem Monat bei.
Stuhltransplantation, andere Krankheiten, die für eine fäkale Bakteriotherapie untersucht wurden
Die Technik wird derzeit bei Patienten mit Parkinson-Krankheit, Diabetes, Fettleibigkeit, Reizdarmsyndrom, chronisch entzündlichen Darmerkrankungen, Multipler Sklerose, idiopathischer thrombozytopenischer Purpura, Morbus Crohn, Insulinresistenz und chronischem Müdigkeitssyndrom untersucht.
Klassisches Verfahren
Üblicherweise wird der Kot eines nahen, gesunden Angehörigen des Patienten nach Untersuchung und Ausschluss von ansteckenden Bakterien oder Viren oder Parasiten wie: Salmonellen, Hepatitis-Virus etc. verwendet.
Nach der Entnahme wird die Stuhlprobe in einem klinischen Labor aufbereitet und in Form einer flüssigen Suspension aufbereitet, die dann über eine nasogastrale Sonde bis auf Höhe des Blinddarms in den oberen Gastrointestinaltrakt instilliert wird.
Das Verfahren umfasst manchmal eine 5-10-tägige Behandlung mit Einläufen, die mit menschlichen Mikrobiota aus dem Kot eines gesunden Spenders hergestellt werden; Die meisten Patienten erholen sich nach nur einer Behandlung.
Die beste Spenderwahl ist ein naher Verwandter, der auf ein breites Spektrum bakterieller und parasitärer Erreger getestet wurde.
Die Einläufe werden in einer Krankenhausumgebung vorbereitet und verabreicht, um die erforderliche Pflege zu gewährleisten.
Die Infusion des Probiotikums kann auch über eine Magensonde erfolgen, wodurch die Bakterien direkt in den Dünndarm gelangen.
Die beiden Methoden können kombiniert werden, um das beste Ergebnis zu erzielen.
Bis zu einem Jahr nach dem Eingriff sollten regelmäßige Kontrolluntersuchungen durchgeführt werden.
ARGF (autologe Wiederherstellung der Magen-Darm-Flora)
Eine modifizierte Form der fäkalen Bakteriotherapie, die derzeit entwickelt wird, ist die autologe Wiederherstellung der gastrointestinalen Flora – (ARGF).
Diese Methode ist sicherer, effektiver und einfacher zu verabreichen.
Eine autologe (eigene) Stuhlprobe wird vom Patienten vor der medizinischen Behandlung abgegeben und im Kühlschrank aufbewahrt.
Wenn der Patient anschließend eine C. difficile-Pathologie entwickelt, wird die Probe mit Kochsalzlösung extrahiert und filtriert. Das Filtrat wird lyophilisiert und der resultierende Feststoff in magensaftresistente Kapseln eingeschlossen.
Durch die Gabe der Kapseln wird die patienteneigene Darmflora wiederhergestellt, was der Bekämpfung einer eventuell eingetretenen C. difficile-Infektion dient.
Dieses Verfahren vermeidet die Risiken der klassischen fäkalen Bakteriotherapie, bei der eine mögliche Infektion durch den Spender auf den Patienten übertragen werden könnte, und vermeidet auch die Notwendigkeit, die Stuhlprobe über eine Magensonde in den Zwölffingerdarm zu verabreichen.
Wirksamkeit
Die Wirksamkeit der Methode zur Verhinderung von Rezidiven der pseudomembranösen Kolitis wird auf etwa 90 % geschätzt.
Eine Studie vom Dezember 2011 bestätigt diese Daten, die bei einer Gruppe von 92 Patienten mit rezidivierenden C.-difficile-Infektionen eine Wirksamkeit der Methode von 26 % bei der Verhinderung von Durchfällen oder weiteren Rezidiven zeigt.
Eine finnische Studie aus dem Jahr 2011 weist darauf hin, dass die antibiotische Behandlung rezidivierender Clostridium-difficile-Infektionen (CDI) bei 50 % der Patienten zu Rezidiven führt.
Die Verwendung einer Stuhltransplantation während eines Koloskopie-Testverfahrens nach einer Darmvorbereitung mit Polyethylenglykol (Lavage) führte zu einer Auflösung von 89 % der Fälle von rezidivierender pseudomembranöser Kolitis nach einem Jahr Nachbeobachtung, was betont, dass die behandelten Fälle verursacht wurden durch a besonders virulenter C. difficile-Stamm (Typ 027).
Ebenfalls im Dezember 2011 zeigte eine Überprüfung von 317 Patienten eine Wirksamkeit der Methode von 92 % bei gleichzeitig geringen Nebenwirkungen.
2015 wurde eine Vergleichsstudie mit Vancomycin veröffentlicht, die die Überlegenheit der bakteriellen Stuhltherapie gegenüber diesem Antibiotikum zeigt.
Lesen Sie auch
Colitis: Symptome, Behandlung und was zu essen
Colitis ulcerosa: Ursachen, Symptome und Behandlung
Die Darmbakterien eines Babys können zukünftige Fettleibigkeit vorhersagen
Kot-Mikrobiota-Transplantation (Kottransplantation): Wozu dient sie und wie wird sie durchgeführt?
Mikrobiota, die Rolle des „Tors“, der das Gehirn vor Darmentzündungen schützt, entdeckt
Was sind die Unterschiede zwischen Divertikulitis und Divertikulose?
Was ist eine Brustnadelbiopsie?
Koloskopie: Die neuesten Techniken und verschiedene Arten
Dysbiose und Hydrokolon-Therapie: So stellen Sie das Darmwohl wieder her
Kapselendoskopie: Was es ist und wie es durchgeführt wird
Koloskopie: Was es ist, wann es gemacht wird, Vorbereitung und Risiken
Colon Wash: Was es ist, wofür es ist und wann es getan werden muss
Rektosigmoidoskopie und Koloskopie: Was sie sind und wann sie durchgeführt werden
Colitis ulcerosa: Was sind die typischen Symptome der Darmerkrankung?
Wales' Sterblichkeitsrate bei Darmoperationen "höher als erwartet"
Reizdarmsyndrom (IBS): Ein gutartiger Zustand, den es unter Kontrolle zu halten gilt
Darminfektionen: Wie wird eine Infektion mit Dientamoeba fragilis übertragen?
Studie findet Verbindung zwischen Dickdarmkrebs und Antibiotika-Einsatz
Darmspiegelung: Effektiver und nachhaltiger mit künstlicher Intelligenz
Kolorektale Resektion: In welchen Fällen die Entfernung eines Dickdarmtrakts erforderlich ist
Gastroskopie: Wozu die Untersuchung dient und wie sie durchgeführt wird
Gastroösophagealer Reflux: Symptome, Diagnose und Behandlung
Endoskopische Polypektomie: Was es ist, wann es durchgeführt wird
Straight Leg Raise: Das neue Manöver zur Diagnose der gastroösophagealen Refluxkrankheit
Gastroenterologie: Endoskopische Behandlung von gastroösophagealem Reflux
Ösophagitis: Symptome, Diagnose und Behandlung
Gastroösophagealer Reflux: Ursachen und Abhilfe
Gastroskopie: Was es ist und wofür es ist
Dickdarmdivertikelkrankheit: Diagnose und Behandlung der Dickdarmdivertikulose
Gastroösophageale Refluxkrankheit (GERD): Symptome, Diagnose und Behandlung
Divertikel: Was sind die Symptome einer Divertikulitis und wie wird sie behandelt?
Reizdarmsyndrom (IBS): Ein gutartiger Zustand, den es unter Kontrolle zu halten gilt
Gastroösophagealer Reflux: Ursachen, Symptome, Tests zur Diagnose und Behandlung
Non-Hodgkin-Lymphom: Symptome, Diagnose und Behandlung einer heterogenen Gruppe von Tumoren
Helicobacter pylori: Wie man es erkennt und behandelt



