باکتری درمانی مدفوع: پیوند مدفوع برای کلستریدیوم دیفیسیل، کولیت و بیماری کرون
باکتری درمانی مدفوع، همچنین به عنوان پیوند مدفوع یا تزریق مدفوع یا تزریق پروبیوتیک های انسانی (HPI) یا پیوند میکروبیوم مدفوع شناخته می شود، یک درمان پزشکی غیردارویی است که در یک فاز آزمایشی با مقداری کارآمدی در افراد مبتلا به کولیت کاذب غشایی متحمل شده توسط باکتری کلستریدیوم دیفیسیل (که اخیراً به «کلستریدیوم دیفیسیل» تغییر نام داده است). یا حتی در موارد کولیت اولسراتیو مقاوم به درمان های رایج
هدف از این درمان ابتکاری، بازیابی اکولوژی میکروبی و هموستاز روده بزرگ با معرفی مجدد یک میکروبیوتای سالم (متعادل) انسانی است که از مدفوع یک اهدا کننده سالم یا در موارد خاص از مدفوعی که قبلاً توسط همان فرد اهدا شده است. هموترانسفوزیون یا ترمیم اتولوگ فلور گوارشی - ARGF).
منطق نظری این روش درمانی را باید در پیشرفتهترین تحقیقات در مورد استفاده از پروبیوتیکها و مطالعات روی میکروبیوم یافت که مجموعهای از میکروارگانیسمها است: باکتریها، باستانباکتریها، قارچها، ویروسها، موجود در یک محیط خاص (در این مورد محیط مدفوع).
به خوبی شناخته شده است که چگونه یک اکولوژی میکروبی خوب می تواند رشد بیش از حد موجودات بیماری زا را دفع کند.
در روده بزرگ تخمین زده می شود که 500 تا 1000 گونه مختلف باکتری با مجموع 1013 باکتری وجود دارد.
در واقع، میکروبیوم را باید به عنوان یک موجود بیولوژیکی به خودی خود در نظر گرفت که همزیست با ارگانیسم میزبان است.
کمپلکس باکتری یا میکروبیوم در حفظ هموستاز ارگانیسم میزبان عمل می کند. این فلور میکروبی وقتی دوباره وارد بدن شود نسبتاً بی ضرر است.
اطلاعات زیادی در مورد نقش میکروبیوم وجود ندارد، با این حال، بسیاری از گونههای حیوانی گیاهخوار و غیر گیاهخوار دارای عادات کوپروفاژیک هستند، احتمالاً به دلیل داشتن چرخه گوارشی دوگانه (هضم مضاعف).
پیوند مدفوع: مزیت اصلی باکتری درمانی مدفوع کاهش خطر ایجاد مقاومت آنتی بیوتیکی در باکتری های بسیار بیماری زا است.
مزایای دیگر هزینه نسبتاً کم، عدم نیاز به دارو و اثربخشی خوب (با وجود مطالعات بزرگتر تأیید می شود) برای درمان مواردی است که مقاومت آنتی بیوتیکی وجود دارد.
با این حال، این روش به دلیل تهاجمی بیشتر آن در مقایسه با درمان مرسوم با آنتیبیوتیکها و خطرات احتمالی انتقال عفونت (باکتریها، ویروسها، پریونها، انگلهای روده) هنوز به عنوان آخرین راهحل در نظر گرفته میشود.
اگرچه تجربه با باکتری درمانی مدفوع هنوز محدود است، نتایج منتشر شده در مورد این روش نشان می دهد که بیش از 80 بیمار میانگین موفقیت بیش از 90٪ را نشان داده اند.
باکتریدرمانی مدفوع، روشی با فناوری پایین و آسان برای انجام است که میتواند چرخههای مصرف مکرر آنتیبیوتیک را بشکند، که به نوبه خود خطر بروز مقاومت آنتیبیوتیکی را کاهش میدهد.
همچنین در مقایسه با تجویز مکرر آنتی بیوتیک با بستری شدن در بیمارستان، پتانسیل صرفه جویی در هزینه ها را دارد.
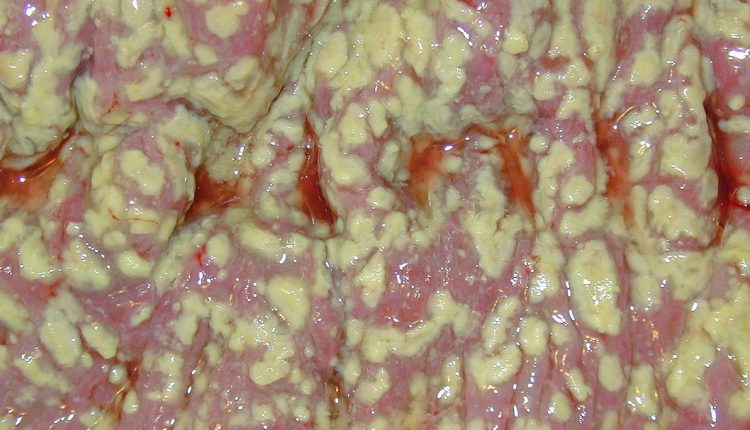
کولیت pseudomembranous
اهمیت به عنوان یک پاتوژن کلستریدیوم دیفیسیل (CDI) از سال 1978 به طور محکم ثابت شده است، اما اهمیت این روش در درمان کولیت کاذب غشایی همچنین از این واقعیت ناشی می شود که اپیدمیولوژی آن اخیراً تغییر کرده و مشکلات تشخیصی و درمانی جدی را برای پزشکان ایجاد کرده است. .
نرخ عفونت (CDI) از 31/100,000 در سال 1996 به 61/100,000 در سال 2003 دو برابر شده است.
در سال های اخیر، شدت و مرگ و میر عفونت C.difficile CDI در حال افزایش بوده است و این به سویه جدید بیماریزای C. difficile که به نام سویه الکتروفورز ژل پالسدار نوع 1 آمریکای شمالی (NAP-1) شناخته می شود نسبت داده شده است. همچنین PFGE نوع BI/NAP1 ریبوتیپ 027.
منحصر به فرد سویه NAP-1 در افزایش تولید سموم A و B و تولید سم دوتایی و مقاومت آن در برابر فلوروکینولون نهفته است.
سویه های NAP1 Hypervirulent C. difficile مسئول اکثر شیوع های اخیر بیمارستانی هستند و استفاده گسترده از آنتی بیوتیک های فلوروکینولون ممکن است تکثیر انتخابی این سویه را تسهیل کرده باشد.
سویه NAP1 همچنین بیشتر احتمال دارد که کولیت شدید و برق آسا ایجاد کند که با لکوسیتوز مشخص، نارسایی حاد کلیه، بی ثباتی همودینامیک و مگاکولون سمی مشخص می شود.
C. difficile به شایع ترین علت باکتریایی اسهال بیمارستانی تبدیل شده است.
عفونت کلستریدیوم دیفیسیل باعث CDAD (بیماری مرتبط با کلستریدیوم دیفیسیل) یا به ندرت کولیت کاذب غشایی می شود که یک وضعیت پزشکی جدی است که باعث عوارض و مرگ و میر قابل توجهی می شود، به ویژه در بیماران تحت درمان با آنتی بیوتیک یا بیماران سرطانی که تحت پیوند سلول های بنیادی قرار می گیرند یا حتی در بیمارانی که تحت رادیوتراپی هستند. .
افزایش فراوانی عفونتها توسط سویههای پر ویروس C. difficile منجر به عوارض و شکستهای درمانی با درمان مرسوم با مترونیدازول و وانکومایسین شده است.
اگرچه با تجربه بالینی محدود، باکتریدرمانی مدفوع در ابتدا نشان داده است که نرخ درمان بالینی بالایی را ارائه میکند، با این حال، آزمایشهای بالینی تصادفیسازی شده برای این رویکرد درمانی تا به امروز وجود ندارد.
کولیت اولسراتیو
در کولیت اولسراتیو تا به امروز هیچ عامل بیماری زایی پیدا نشده است.
اما اثربخشی باکتری درمانی مدفوع در این مورد نشان می دهد که علت کولیت اولسراتیو ممکن است به دلیل عفونت قبلی با یک پاتوژن باشد که ناشناخته مانده است.
در واقع، احتمالاً عفونت اولیه در این بیماران به طور طبیعی برطرف شده است. اما گاهی اوقات، عدم تعادل در فلور روده روده بزرگ ممکن است منجر به شعله ور شدن التهاب شود (که ماهیت چرخه ای و عود کننده این بیماری را توضیح می دهد).
به نظر می رسد این چرخه، حداقل در بسیاری از موارد، با استعمار مجدد کولون بیمار با یک کمپلکس باکتریایی (پروبیوتیک) گرفته شده از روده سالم (هتروگرافت) قطع می شود.
برخی از پزشکان معتقدند که این درمان که در افراد سالم انجام می شود بی خطر است و بسیاری از بیماران می توانند از این درمان ابتکاری بهره مند شوند.
مطالعه ای در می 2011، تمایل خوب بیماران و والدین کودکان مبتلا به کولیت اولسراتیو را برای پذیرش این درمان، پس از غلبه بر انزجار اولیه خود از این روش، تأیید کرد.
در سال 2013، تحقیق دیگری اعتبار درمان را با یک مطالعه آزمایشی آینده نگر بر روی ده فرد 7 تا 21 ساله تایید کرد.
این مطالعه تحمل و اثربخشی درمان پیوند مدفوع را در کولیت اولسراتیو نشان میدهد. در واقع، در هفت مورد بهبودی بالینی در یک هفته و شش نفر از نه نفر بهبودی بالینی را در یک ماه حفظ کردند.
پیوند مدفوع، سایر بیماری های مورد مطالعه برای باکتری درمانی مدفوع
این تکنیک در حال حاضر در افراد مبتلا به بیماری پارکینسون، دیابت، چاقی، سندرم روده تحریک پذیر، بیماری التهابی مزمن روده، مولتیپل اسکلروزیس، پورپورای ترومبوسیتوپنیک ایدیوپاتیک، بیماری کرون، مقاومت به انسولین و سندرم خستگی مزمن در حال بررسی است.
روش کلاسیک
معمولاً مدفوع یکی از بستگان نزدیک و سالم بیمار پس از بررسی و رد وجود باکتری های مسری یا ویروس ها یا انگل هایی مانند: سالمونلا، ویروس هپاتیت و غیره استفاده می شود.
پس از جمع آوری، نمونه مدفوع به صورت سوسپانسیون مایع در آزمایشگاه بالینی پردازش و آماده می شود و سپس از طریق لوله بینی معده ای که تا سطح سکوم بالا می رود، به دستگاه گوارش فوقانی تزریق می شود.
این روش گاهی شامل 5 تا 10 روز درمان با تنقیه است که با میکروبیوتای انسانی از مدفوع یک اهداکننده سالم ساخته شده است. اکثر بیماران تنها پس از یک درمان بهبود می یابند.
بهترین انتخاب اهداکننده، یکی از بستگان نزدیک است که برای طیف وسیعی از عوامل باکتریایی و انگلی آزمایش شده باشد.
تنقیه ها برای اطمینان از تمام مراقبت های لازم در محیط بیمارستان تهیه و اجرا می شوند.
تزریق پروبیوتیک همچنین می تواند از طریق لوله بینی معده انجام شود و باکتری ها را مستقیماً به روده کوچک برساند.
این دو روش را می توان برای دستیابی به بهترین نتیجه ترکیب کرد.
معاینات منظم باید تا یک سال پس از عمل انجام شود.
ARGF (ترمیم اتولوگ فلور دستگاه گوارش)
یک شکل اصلاح شده از باکتری درمانی مدفوع، که در حال حاضر در حال توسعه است، ترمیم اتولوگ فلور گوارشی - (ARGF) است.
این روش ایمن تر، موثرتر و اجرا آسان تر است.
نمونه مدفوع اتولوگ (خود) قبل از درمان پزشکی توسط بیمار تهیه می شود و در یخچال نگهداری می شود.
اگر بیمار متعاقباً دچار آسیب شناسی C. difficile شود، نمونه با سالین استخراج و فیلتر می شود. فیلتر لیوفیلیزه می شود و جامد حاصل در کپسول های مقاوم در برابر معده محصور می شود.
تجویز کپسول ها فلور روده بزرگ خود بیمار را بازیابی می کند، که در مبارزه با عفونت C. difficile که ممکن است ایجاد شده باشد مفید است.
این روش از خطرات باکتریدرمانی مدفوع کلاسیک، که در آن عفونت احتمالی میتواند توسط اهداکننده به بیمار منتقل شود، جلوگیری میکند و همچنین از نیاز به تزریق نمونه مدفوع به دوازدهه از طریق پروب معده جلوگیری میکند.
اثر
اثربخشی روش در پیشگیری از عود کولیت کاذب غشایی حدود 90 درصد برآورد شده است.
مطالعه ای از دسامبر 2011 این داده ها را تأیید می کند که نشان می دهد اثربخشی روش 92 درصد در پیشگیری از اسهال یا عود بیشتر در گروه 26 بیمار مبتلا به عفونت های مکرر C. difficile را نشان می دهد.
یک مطالعه فنلاندی در سال 2011 نشان می دهد که درمان آنتی بیوتیکی عفونت های مکرر کلستریدیوم دیفیسیل (CDI) منجر به عود در 50٪ از بیماران می شود.
استفاده از پیوند مدفوع در طی یک روش تست کولونوسکوپی پس از آماده سازی روده با پلی اتیلن گلیکول (لاواژ) منجر به رفع 89 درصد از موارد کولیت کاذب غشایی راجعه در پیگیری یک ساله شد، با تاکید بر اینکه موارد درمان شده ناشی از به ویژه سویه C. difficile خطرناک (نوع 027).
همچنین در دسامبر 2011، بررسی 317 بیمار، 92 درصد کارایی روش را نشان داد، همچنین عوارض جانبی کمی را نشان داد.
در سال 2015، مطالعه مقایسه ای با وانکومایسین منتشر شد که نشان دهنده برتری مدفوع درمانی باکتریایی نسبت به این آنتی بیوتیک بود.
همچنین بخوانید
Emergency Live Even More… Live: دانلود برنامه رایگان جدید روزنامه شما برای IOS و Android
کولیت: علائم، درمان و آنچه باید بخوریم
کولیت اولسراتیو: علل، علائم و درمان
باکتری های روده کودک ممکن است چاقی آینده را پیش بینی کند
پیوند میکروبیوتای مدفوع (پیوند مدفوع): برای چیست و چگونه انجام می شود؟
سنت اورسولا در بولونیا (ایتالیا) مرز پزشکی جدیدی را با پیوند میکروبیوتا باز کرد
کشف میکروبیوتا ، نقش "دروازه" که از مغز در برابر التهاب روده محافظت می کند
تفاوت بین دیورتیکولیت و دیورتیکولوز چیست؟
کولونوسکوپی: جدیدترین تکنیک ها و انواع مختلف
دیسبیوز و هیدروکلون تراپی: چگونه سلامت روده را بازیابی کنیم
آندوسکوپی کپسولی: چیست و چگونه انجام می شود
کولونوسکوپی: چیست، چه زمانی انجام شود، آماده سازی و خطرات
کولون واش: چیست، چه کاری انجام می شود و چه زمانی باید انجام شود
رکتوسیگموئیدوسکوپی و کولونوسکوپی: چه هستند و چه زمانی انجام می شوند
کولیت اولسراتیو: علائم بارز بیماری روده چیست؟
نرخ مرگ جراحی روده ولز "بالاتر از حد انتظار"
سندرم روده تحریک پذیر (IBS): یک وضعیت خوش خیم برای کنترل
عفونت های روده ای: عفونت دیانتامبا فراگیلیس چگونه ایجاد می شود؟
مطالعه ارتباط بین سرطان روده بزرگ و مصرف آنتی بیوتیک را پیدا می کند
کولونوسکوپی: موثرتر و پایدارتر با هوش مصنوعی
رزکسیون کولورکتال: در چه مواردی برداشتن کولون ضروری است
گاستروسکوپی: معاینه برای چیست و چگونه انجام می شود
رفلاکس معده- مری: علائم، تشخیص و درمان
پولیپکتومی آندوسکوپی: چیست، چه زمانی انجام می شود
بلند کردن مستقیم پا: مانور جدید برای تشخیص بیماری رفلاکس معده- مری
گوارش: درمان آندوسکوپی برای رفلاکس معده- مری
ازوفاژیت: علائم، تشخیص و درمان
بیماری دیورتیکول کولون: تشخیص و درمان دیورتیکولوز کولون
بیماری رفلاکس معده و مری (GERD): علائم، تشخیص و درمان
دیورتیکول: علائم دیورتیکولیت چیست و چگونه آن را درمان کنیم
سندرم روده تحریک پذیر (IBS): یک وضعیت خوش خیم برای کنترل
رفلاکس معده: علل ، علائم ، آزمایشات تشخیص و درمان
لنفوم غیر هوچکین: علائم، تشخیص و درمان یک گروه ناهمگن از تومورها
هلیکوباکتر پیلوری: چگونه آن را بشناسیم و درمان کنیم



